Фармакологические характеристики
В настоящее время производится достаточно много недеполяризующих препаратов (табл. 9-6). Выбор недеполяризующего миорелаксанта зависит от индивидуальных свойств препарата, которые во многом определяются его структурой. Например, стероидные соединения дают ваголитический эффект (т. е. подавляют функцию блуждающего нерва), а бензохинолины высвобождают гистамин из тучных клеток.
А. Влияние на вегетативную нервную систему. Недеполяризующие миорелаксанты в клинических дозах по-разному влияют на н- и м-холинорецепторы. Тубокурарин и, в меньшей степени, метокурин блокируют вегетативные ганглии, что ослабляет опосредованное симпатической нервной системой увеличение ЧСС и сократимости миокарда при артериальной гипотонии и других видах операционного стресса. Панкуроний и гал-ламин, наоборот, блокируют м-холинорецепторы синоатриального узла, что вызывает тахикардию.
ТАБЛИЦА 9-6. Фармакология недеполяризующих миорелаксантов
Примечание. Начало действия: + - медленное; ++ - умеренно быстрое; +++ - быстрое.
Длительность действия: + - препарат короткого действия; ++ - препарат средней продолжительности действия;
Препарат длительного действия.
Высвобождение гистамина: О - отсутствует; + - незначительное; ++ - средней интенсивности; +++ - значительное.
Блокада блуждающего нерва: О - отсутствует; + - незначительная; ++ - средней степени.
2 Базируется на средней оптовой цене за 1 мл препарата, что не во всех случаях отражает силу и длительность действия.
Мощный ваголитический эффект галламина (ограниченный холинорецепторами сердца.- Примеч. пер.) значительно сузил его клиническое применение. При использовании в рекомендованных дозах атракурий, мивакурий, доксакурий, векуро-ний и пипекуроний не оказывают значительного влияния на вегетативную нервную систему.
Б. Высвобождение гистамина. Высвобождение гистамина из тучных клеток может вызывать бронхоспазм, покраснение кожи и артериальную гипотонию вследствие периферической вазодила-тации. Степень высвобождения гистамина по убывающей представлена следующим образом: тубо-курарин > метокурин > атракурий и мивакурий. Медленная скорость введения и предварительное использование H1- и Н2-блокаторов устраняет эти побочные эффекты.
В. Печеночный клиренс. Только панкуроний и векуроний подвергаются интенсивному метаболизму в печени. Основной путь выведения векуро-ния и рокурония - через желчь. Печеночная недостаточность удлиняет действие панкурония и рокурония, но слабее влияет на векуроний. Атракурий и мивакурий подвергаются интенсивному внепеченочному метаболизму.
Г. Почечная экскреция. Элиминация метокурина и галламина почти полностью зависит от почечной экскреции, поэтому данные препараты противопоказаны при почечной недостаточности. Однако метокурин и галламин ионизированы, поэтому их можно удалить с помощью гемодиализа. Тубокурарин, доксакурий, панкуроний, векуроний и пипекуроний только частично выделяются через почки, поэтому почечная недостаточность удлиняет их действие. Элиминация атракурия и миваку-рия не зависит от функции почек.
Д. Возможность применения для интубации трахеи. Только рокуроний вызывает нервно-мышечный блок так же быстро, как сукцинилхолин. Развитие эффекта недеполяризующих миорелаксантов можно ускорить, применяя их в высоких или насыщающих дозах. Хотя высокая доза убыстряет наступление миорелаксации, одновременно она усугубляет побочные эффекты и увеличивает продолжительность действия. Например, при введении панкурония в дозе 0,15 мг/кг интубировать трахею можно уже через 90 с, но при этом возникают выраженная артериальная гипертония и тахикардия, а продолжительность необратимого блока может превысить 45 мин.
Появление препаратов средней продолжительности действия (атракурий, векуроний, рокуроний) и короткого действия (мивакурий) привело к широкому распространению введения миорелаксантов в два приема с использованием насыщающей дозы. Теоретически введение 10-15 % стандартной дозы для интубации за 5 мин до индукции анестезии вызывает блокаду значительного числа н-холинорецепторов, так что при последующей инъекции оставшейся дозы быстро возникает миорелаксация. Насыщающая доза, как правило, не вызывает клинически значимого паралича скелетных мышц, потому что для этого требуется блокада 75-80 % рецепторов (нервно-мышечная граница безопасности). Тем не менее в некоторых случаях насыщающая доза блокирует достаточно большое число рецепторов, что приводит к одышке и дисфагии. В этом случае больного нужно успокоить и быстро провести индукцию анестезии. При дыхательной недостаточности насыщающая доза может значительно ухудшить респираторную функцию и снизить количество оксигемоглобина. Насыщающая доза позволяет интубировать трахею через 60 с после введения основной дозы рокурония и через 90 с после введения основной дозы остальных миорелаксантов средней продолжительности действия. Рокуроний - это недеполяризующий миорелаксант выбора для быстрой последовательной индукции, поскольку он быстро вызывает миорелаксацию, не влечет значительных побочных эффектов даже при использовании больших доз и имеет среднюю продолжительность действия.
E. Фасцикуляции. Для предотвращения фасцикуляций за 5 мин до сукцинилхолина вводят 10-15 % стандартной дозы недеполяризующего миорелаксанта для интубации (прекураризация). Для этой цели можно применять подавляющее большинство недеполяризующих миорелаксантов, наиболее эффективным из которых является тубо-курарин. Так как недеполяризующие миорелаксанты являются антагонистами I фазы деполяризующего блока, то доза сукцинилхолина должна быть высокой (1,5 мг/кг).
Ж. Потенцирующий эффект ингаляционных анестетиков. Ингаляционные анестетики снижают потребность в недеполяризующих миорелаксантах не менее чем на 15 %. Степень постсинапти-ческого потенцирования зависит как от применяемого анестетика (изофлюран, севофлю-ран, десфлюран и энфлюран > галотан > закись азота/кислород/опиат), так и от используемого миорелаксанта (тубокурарин и панкуроний > векуроний и атракурий).
3. Потенцирующий эффект других недеполяризующих миорелаксантов: сочетание некоторых недеполяризующих миорелаксантов (например, тубокурарина и панкурония) вызывает не аддитивный, а потенцирующий эффект. Дополнительным преимуществом некоторых комбинаций явля-
Ется уменьшение побочных эффектов: например, панкуроний ослабляет гипотензивное действие ту-бокурарина. Отсутствие потенцирования при взаимодействии миорелаксантов со сходной структурой (например, векурония и панкурония) вызвало к жизни теорию, что потенцирование возникает в результате незначительных различий в механизме действия.
Влияние некоторых параметров на фармакологические свойства недеполяризующих миорелаксантов
А. Температура. Гипотермия удлиняет нервно-мышечный блок вследствие угнетения метаболизма (например, мивакурий, атракурий) и замедления экскреции (например, тубокурарин, метокурин, панкуроний).
Б. Кислотно-основное равновесие. Респираторный ацидоз потенцирует действие большинства недеполяризующих миорелаксантов и угнетает восстановление нервно-мышечной проводимости ингибиторами ацетилхолинэстеразы. Следовательно, гиповентиляция в послеоперационном периоде препятствует полному восстановлению нервно-мышечной проводимости. Сведения о влиянии других расстройств кислотно-основного равновесия носят противоречивый характер из-за сопутствующих изменений рН внеклеточной жидкости, внутриклеточного рН, концентрации электролитов и структурных различий между миорелаксантами (например, моно- и бисчетвертичные аммониевые соединения; стероидные релаксанты и бензохинолины).
В. Электролитные расстройства. Гипокалиемия и гипокальциемия потенцируют недеполяризующий блок. Влияние гиперкальциемии непредсказуемо. Гипермагниемия, которая может возникать при лечении преэклампсии магния сульфатом, потенцирует недеполяризующий блок вследствие конкурирования с кальцием в концевых пластинках скелетных мышц.
Г. Возраст. Новорожденные имеют повышенную чувствительность к миорелаксантам вследствие незрелости нервно-мышечных синапсов. Однако эта гиперчувствительность необязательно вызывает снижение потребности в миорелаксантах - большое внеклеточное пространство у новорожденных увеличивает объем распределения.
Д. Взаимодействие с лекарственными средствами. Как уже отмечалось, многие препараты потенцируют недеполяризующий блок (табл. 9-4). Взаимодействие происходит на различных уровнях: пресинаптические структуры, постсинаптические холинорецепторы, мембраны мышечных клеток.
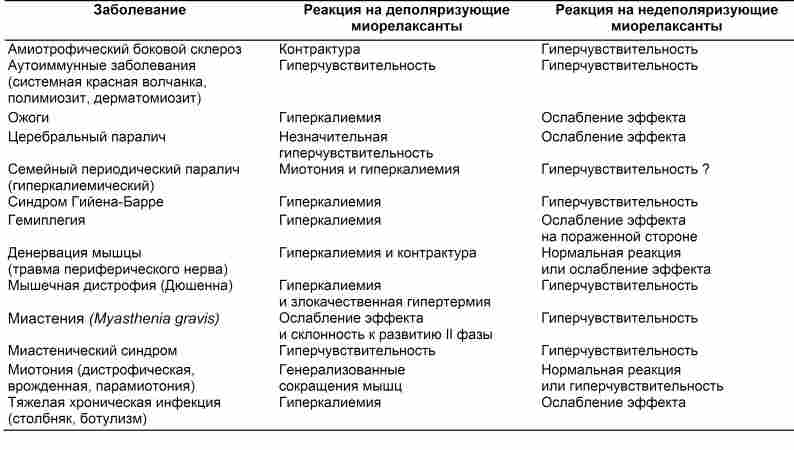
E. Сопутствующие заболевания. Заболевания нервной системы и мышц оказывают глубокое влияние на действие миорелаксантов (табл. 9-7). Цирроз печени и хроническая почечная недостаточность часто увеличивают объем распределения и уменьшают концентрацию в плазме таких водорастворимых препаратов, как миорелаксанты. Одновременно увеличивается продолжительность действия препаратов, метаболизм которых зависит от печеночной и почечной экскреции. Таким образом, при циррозе печени и хронической почечной недостаточности целесообразно использовать более высокую начальную (нагрузочную) дозу миорелаксанта и меньшую поддерживающую (по сравнению со стандартными условиями).
Ж. Реакция различных групп мышц. Начало миорелаксации и ее длительность широко варьируются в разных группах мышц. Эта вариабельность может быть обусловлена неравномерным кровотоком, различным расстоянием до крупных сосудов, неодинаковым составом волокон. Более того, относительная чувствительность групп мышц различается при использовании разных миорелаксантов. При введении недеполяризующих миорелаксантов в диафрагме, мышцах гортани и в круговой мышце глаза миорелаксация наступает и исчезает быстрее, чем в мышцах большого пальца кисти. При этом диафрагма может сокращаться даже при полном отсутствии реакции отводящей мышцы большого пальца кисти на стимуляцию локтевого нерва (являясь дополнительной гарантией безопасности, эта особенность дезориентирует анестезиолога). Мышцы голосовой щели могут быть резистентны к действию миорелаксантов, что часто и наблюдают при ларингоскопии.
На длительность и глубину миорелаксации влияет множество факторов, поэтому для оценки действия миорелаксантов необходимо проводить мониторинг нервно-мышечной проводимости. Рекомендованные дозы, включая приведенные в настоящей главе, являются ориентировочными и требуют коррекции в зависимости от индивидуальной чувствительности.
Тубокурарин
Структура
Тубокурарин (d-тубокурарин) - это моночетвертичное аммониевое соединение, содержащее третичную аминогруппу (рис. 9-3). Четвертичная аммониевая группа имитирует положительно заряженный участок молекулы ацетилхолина и, следовательно, отвечает за связывание с рецептором, в то время как крупная кольцевидная часть молекулы тубокурарина препятствует стимуляции рецептора.
ТАБЛИЦА 9-7. Заболевания, при которых изменяется реакция на миорелаксанты
Метаболизм и экскреция
Тубокурарин не подвергается значительному метаболизму. Элиминация происходит в основном через почки (в первые 24 ч выделяется 50 % препарата) и, в меньшей степени, с желчью (10 %). Наличие почечной недостаточности удлиняет действие препарата.
Дозировка
Доза тубокурарина, необходимая для проведения интубации, составляет 0,5-0,6 мг/кг, ее вводят медленно в течение 3 мин. Интраоперационная релаксация достигается нагрузочной дозой 0,15 мг/кг, что сменяется дробным введением по 0,05 мг/кг. При массе тела 70 кг это соответствует нагрузочной дозе 9 мг, затем каждые 20-30 мин вводят по 3 мг препарата.
У детей потребность в нагрузочной дозе не ниже, в то время как интервалы между введением поддерживающих доз препарата длиннее. Чувствительность новорожденных к тубокурарину значительно
Варьируется. Тубокурарин выпускают по 3 мг в 1 мл раствора. Хранят при комнатной температуре.
А. Артериальная гипотония и тахикардия. Возникают в первую очередь вследствие высвобождения гистамина. Влияние тубокурарина на вегетативные ганглии играет второстепенную роль.
Б. Бронхоспазм. Обусловлен высвобождением гистамина. Тубокурарин не следует использовать при бронхиальной астме.
Метокурин
Структура
Метокурин - это бисчетвертичное производное тубокурарина, его еще называют диметилтубокурарином. Сходство многих фармакологических характеристик и побочных эффектов тубокурарина и метокурина обусловлено структурной аналогией.
Метаболизм и экскреция
Подобно тубокурарину метокурин не подвергается метаболизму и выделяется в основном через
Почки (50 % препарата в первые 24 ч). Наличие почечной недостаточности удлиняет действие препарата. Экскреция с желчью играет незначительную роль (
Дозировка
Интубация возможна при введении препарата в дозе 0,3 мг/кг. Медленное введение на протяжении 1-2 мин сводит к минимуму побочные эффекты. Нагрузочная доза для интраоперационной миорелаксации - 0,08 мг/кг, поддерживающая - 0,03 мг/кг.
Особенности применения тубокурарина в педиатрии распространяются и на применение мето-курина. Вне зависимости от возраста, мощность метокурина в 2 раза выше, чем у тубокурарина.
Побочные эффекты и особенности применения
Введение метокурина в дозах, равноэффективных дозам тубокурарина, вызывает высвобождение вдвое меньшего количества гистамина. Тем не менее при введении высоких доз возникают артериальная гипотония, тахикардия, бронхоспазм и аллергические реакции. Аллергия к йоду (которая имеется, например, при аллергии к рыбе) - противопоказание к применению, потому что препарат содержит йод.
Атракурий Структура
В состав атракурия, что характерно для всех миорелаксантов, входит четвертичная аммониевая группа. Вместе с тем, бензохинолиновая структура атракурия обеспечивает метаболизм препарата.
Метаболизм и экскреция
Метаболизм атракурия настолько интенсивен, что его фармакокинетика не зависит от состояния функции печени и почек: в неизмененном виде с мочой и желчью выделяется менее 10 % препарата. Метаболизм обеспечивается двумя независимыми процессами.
А. Гидролиз эфирной связи. Этот процесс катализируют неспецифические эстеразы, причем ацетилхолинэстераза и псевдохолинэстераза не имеют к нему отношения.
Б. Элиминация Хоффмана. При физиологических значениях рН и температуры тела атракурий подвергается спонтанному неферментативному химическому разрушению.
Дозировка
Доза, необходимая для проведения интубации, составляет 0,5 мг/кг, ее вводят в течение 30-60 с. Нагрузочная доза для интраоперационной миорелаксации - 0,25 мг/кг, поддерживающая - 0,1 мг/кг каждые 10-20 мин. Инфузия в дозе 5-10 мкг/(кг х мин) - полноценная замена дробного введения.
Хотя потребность в препарате мало зависит от возраста пациента, длительность действия атракурия у детей все же меньше таковой у взрослых.
Атракурий выпускают в виде растворов, содержащих 10 мг в 1 мл. Препарат следует хранить в холодильнике при температуре 2-8 0C, так как каждый месяц хранения при комнатной температуре снижает его мощность на 5-10 %.
Побочные эффекты и применение в клинике
По сравнению с тубокурарином и метокурином атракурий высвобождает гистамин в меньшей степени.
А. Артериальная гипотония и тахикардия. Побочные эффекты в отношении системы кровообращения возникают редко при условии, что доза препарата не превышает 0,5 мг/кг. Атракурий также способен вызывать преходящее снижение ОПСС и увеличение сердечного индекса независимо от высвобождения гистамина. Медленный темп инъекции уменьшает выраженность этих побочных эффектов.
Б. Бронхоспазм. Атракурий не следует применять при бронхиальной астме. Более того, атракуриум может вызвать тяжелый бронхоспазм, даже если в анамнезе нет бронхиальной астмы.
В. Токсичность лауданозина. Лауданозин - продукт метаболизма атракурия, образующийся при элиминации Хоффмана. Лауданозин возбуждает ЦНС, что увеличивает потребность в анестетиках (повышается МАК) и даже провоцирует судороги. Выраженность этих эффектов в подавляющем большинстве случаев не достигает клинической значимости; исключения возникают при использовании чрезмерно высокой общей дозы препарата или при печеночной недостаточности (лауданозин подвергается метаболизму в печени).
Г. Чувствительность к температуре тела и рН. Гипотермия и ацидоз ингибируют элиминацию Хоффмана, что удлиняет действие атракурия.
Д. Химическая несовместимость. Если атракурий вводят в систему для внутривенных инфузий, содержащую щелочной раствор (например, тиопентал), то он, являясь кислотой, выпадает в осадок.
Цисатракурий Структура
Цисатракурий - это новый недеполяризующий ре-лаксант, являющийся изомером атракурия. В настоящее время проходят испытания этого препарата.
Метаболизм и экскреция
При физиологических значениях рН и температуры тела Цисатракурий, подобно атракурию, подвергается элиминации Хоффмана. В результате этой реакции возникают метаболиты (моночетвертичный акриулат и лауданозин), которые не вызывают нервно-мышечный блок. Неспецифические эстеразы не участвуют в метаболизме цисатракурия. Наличие почечной и печеночной недостаточности не влияет на метаболизм и элиминацию цисатракурия.
Дозировка
Доза для интубации составляет 0,1-0,15 мг/кг, ее вводят в течение 2 мин, что вызывает нервно-мышечную блокаду средней продолжительности действия. Инфузия в дозе 1-2 мкг/(кг х мин) позволяет поддержать интраоперационную миорелаксацию. Таким образом, Цисатракурий равно-эффективен векуронию.
Цисатракурий следует хранить в холодильнике при температуре 2-8 0C. После извлечения из холодильника и при хранении при комнатной температуре препарат следует использовать в течение 21 дня.
Побочные эффекты и особенности применения
Цисатракурий, в отличие от атракурия, не вызывает стойкого дозозависимого увеличения содержания гистамина в плазме. Цисатракурий не влияет на ЧСС, артериальное давление и вегетативную нервную систему даже в дозе, превышающей ЛД 95 в 8 раз.
Токсичность лауданозина, чувствительность к температуре тела и рН и химическая несовместимость, характерные для атракурия, в равной степени свойственны и цисатракурию.
Мивакурий Структура
Мивакурий является производным бензохинолина.
Метаболизм и экскреция
Мивакурий, подобно сукцинилхолину, гидролизу -ется псевдохолинэстеразой. Истинная холинэстераза принимает крайне незначительное участие в метаболизме мивакурия. Следовательно, если концентрация псевдохолинэстеразы снижена (табл. 9-3) или она представлена атипичным вариантом, то продолжительность действия мивакурия существенно увеличится. При гетерозиготном дефектном гене псевдохолинэстеразы блок длится в 2-3 раза дольше обычного, при гомозиготном - может сохраняться часы. Так как при гомозиготном дефекте псевдохолинэстераза не подвергает метаболизму мивакурий, то продолжительность нервно-мышечного блока становится аналогичной таковой при введении миорелаксантов длительного действия. В отличие от сукцинилхолина ингибиторы ацетилхолинэстеразы устраняют миопа-ралитический эффект мивакурия при наличии хотя бы слабого мышечного ответа на стимуляцию нерва. Несмотря на то, что метаболизм мивакурия напрямую не зависит от состояния функции печени или почек, длительность его действия при наличии печеночной или почечной недостаточности увеличивается вследствие снижения концентрации псевдохолинэстеразы в плазме.
Дозировка
Доза, необходимая для проведения интубации, составляет 0,15-0,2 мг/кг. Инфузия в начальной дозе 4-10 мкг/(кг х мин) позволяет обеспечить интраоперационную миорелаксацию. Точная доза зависит от концентрации псевдохолинэстеразы в плазме. В пересчете на массу тела детям необходимы более высокие дозы препарата, чем взрослым (в пересчете на площадь поверхности тела дозы одинаковы).
Побочные эффекты и особенности применения
Мивакурий высвобождает гистамин в количественном отношении аналогично атракурию. Медленное введение препарата (в течение 1 мин) позволяет свести к минимуму обусловленную выбросом гистамина артериальную гипотонию и тахикардию. Тем не менее если доза мивакурия превышает 0,15 мг/кг, то при заболеваниях сердца даже медленное введение препарата не предотвращает резкого снижения артериального давления. Начало действия мивакурия аналогично таковому атракурия (2-3 мин). Главное преимущество мивакурия - короткая продолжительность действия (20-30 мин), что в 2-3 раза дольше I фазы сукци-нилхолинового блока, но в 2 раза короче продолжительности действия атракурия, векурония и ро-курония. У детей препарат начинает действовать быстрее, а продолжительность действия короче, чем у взрослых. Мивакурий можно хранить при комнатной температуре 18 мес.
Доксакурий
Структура
Доксакурий - бензохинолиновое соединение, по структуре напоминающее мивакурий и атракурий.
Метаболизм и экскреция
Этот мощный миорелаксант длительного действия лишь незначительно гидролизуется холинэстеразой плазмы. Как и у других миорелаксантов длительного действия, главным путем элиминации является экскреция через почки. При наличии болезней почек длительность действия доксакурия увеличивается. Экскреция с желчью не играет значительной роли в элиминации доксакурия.
Дозировка
Доза, необходимая для проведения интубации, составляет 0,05 мг/кг. Интубацию можно выполнять через 5 мин после введения. Нагрузочная доза для интраоперационной миорелаксации - 0,02 мг/кг, поддерживающие дробные дозы - 0,005 мг/кг. Дозы доксакурия у детей и пожилых в пересчете на массу тела аналогичны названным выше, хотя в преклонном возрасте доксакурий действует дольше.
Побочные эффекты и особенности применения
Доксакурий не высвобождает гистамин и не влияет на кровообращение. Он начинает действовать немного медленнее, чем остальные недеполяризующие миорелаксанты длительного действия (через 4-6 мин), в то время как продолжительность эффекта аналогична таковой панкурония (60-90 мин).
Панкуроний
Структура
Панкуроний состоит из стероидного кольца, к которому присоединены две модифицированные молекулы ацетилхолина (бисчетвертичное аммониевое соединение). Панкуроний связывается с холинорецептором, но не стимулирует его.
Метаболизм и экскреция
В отличие от тубокурарина и метокурина панкуро-ний в некоторой степени подвергается метаболизму в печени (деацетилирование). Продукт метаболизма тоже дает миопаралитический эффект. Экскреция происходит в основном через почки (40 %), в меньшей степени с желчью (10 %). Естественно, при наличии почечной недостаточности элиминация панкурония замедляется и нервно-мышечный блок удлиняется. При циррозе печени из-за повышенного объема распределения необходимо увеличить начальную дозу, но поддерживающая доза снижается вследствие низкого клиренса.
Дозировка
Мощность панкурония наполовину меньше, чем у доксакурия. Через 2-3 мин после введения панкурония в дозе 0,08-0,12 мг/кг можно интубировать трахею. Нагрузочная доза для интраоперационной миорелаксации - 0,04 мг/кг, поддерживающая доза - 0,01 мг/кг каждые 20-40 мин.
У детей потребности в панкуронии немного выше.
Панкуроний выпускают в виде раствора, 1 мл которого содержит 1-2 мг препарата. Панкуроний следует хранить в холодильнике при температуре 2-8 0C.
Побочные эффекты и особенности применения
А. Артериальная гипертония и тахикардия. Влияние панкурония на кровообращение обусловлено блокадой блуждающего нерва и высвобождением катехоламинов из окончаний адренергических нервов. Панкуроний следует применять с осторожностью в тех случаях, когда развитие тахикардии является фактором повышенного риска (ИБС, гипертрофическая кардиомиопатия).
Б. Аритмии. Повышение атриовентрикуляр-ной проводимости и высвобождение катехоламинов увеличивают вероятность желудочковых аритмий у больных в группе риска. Особенно высок риск аритмии при сочетании панкурония, трицик-лических антидепрессантов и галотана.
В. Аллергические реакции. При гиперчувствительности к бромидам может возникнуть аллергия на панкуроний (панкуронии бромид).
Векуроний
Структура
Векуроний - это панкуроний без четвертичной метиловой группы (т. е. он представляет собой моночетвертичное аммониевое соединение). Незначительное структурное отличие уменьшает выраженность побочных эффектов, не влияя на мощность.
Метаболизм и экскреция
В незначительной степени метаболизм векурония происходит в печени. Векуроний выделяется главным образом с желчью, в меньшей степени через почки (25 %). Векуроний целесообразно использовать при почечной недостаточности, хотя иногда это состояние удлиняет действие препарата. Кратковременность действия векурония объясняется более коротким периодом полусуществования в фазе элиминации и более быстрым клиренсом по сравнению с панкуронием. Длительное применение векурония в отделениях интенсивной терапии вызывает у пациентов продолжительный нервно-мышечный блок (до нескольких дней), возможно вследствие накопления 3-гидрокси-метаболита или же из-за развития полинейропатии. К факторам риска относят принадлежность к женскому полу, наличие почечной недостаточности, длительный прием кор-тикостероидов и сепсис. Действие векурония удлиняется при СПИДе. При длительном применении развивается толерантность к препарату.
Дозировка
Векуроний равноэффективен панкуронию. Доза, необходимая для проведения интубации, составляет 0,08-0,12 мг/кг. Нагрузочная доза для интраоперационной миорелаксации - 0,04 мг/кг, поддерживающая доза - 0,01 мг/кг каждые 15-20 мин. Инфузия в дозе 1-2 мкг/(кг х мин) тоже позволяет добиться хорошей релаксации.
Возраст не влияет на потребности в нагрузочной дозе, в то время как интервалы между приемом поддерживающих доз у новорожденных и грудных детей должны быть длиннее. Длительность действия векурония увеличивается у только что родивших женщин вследствие изменений печеночного кровотока и поглощения препарата печенью.
Векуроний расфасован по 10 мг в виде порошка, который растворяют в свободной от консервантов воде непосредственно перед введением. Разведенный препарат можно использовать в течение 24 ч.
Побочные эффекты и особенности применения
А. Кровообращение. Даже в дозе 0,28 мг/кг веку-роний не оказывает влияния на кровообращение.
Б. Печеночная недостаточность. Хотя элиминация векурония определяется экскрецией с желчью, наличие печеночной недостаточности незначительно увеличивает длительность действия препарата - при условии, что доза не превышает 0,15 мг/кг. В ангепатическую фазу трансплантации печени потребность в векуронии снижается.
Пипекуроний
Структура
Пипекуроний - бисчетвертичное аммониевое соединение стероидной структуры, очень сходное с панкуронием.
Метаболизм и экскреция
Как и у других недеполяризующих миорелаксантов длительного действия, метаболизм играет незначительную роль в элиминации пипекурония. Элиминация определяется экскрецией, которая происходит в основном через почки (70 %) и с желчью (20 %). Длительность действия увеличивается у больных с почечной, но не с печеночной недостаточностью.
Дозировка
Пипекуроний немного более мощный препарат, чем панкуроний. Доза, необходимая для проведения интубации, составляет 0,06-0,1 мг/кг. Дозы для интраоперационного поддержания миорелаксации на 20 % ниже, чем у панкурония. У грудных детей потребность в препарате в пересчете на килограмм массы тела выше, чем у старших детей и взрослых. Пожилой возраст практически не влияет на фармакологический профиль пипекурония.
Побочные эффекты и особенности применения
Главное преимущество пипекурония над панкуронием - отсутствие побочного влияния на кровообращение. Пипекуроний не вызывает высвобождения гистамина. Начало и длительность действия у этих препаратов схожи.
Рокуроний
Структура
Этот моночетвертичный стероидный аналог векурония был синтезирован таким образом, чтобы обеспечить быстрое начало действия.
Метаболизм и экскреция
Рокуроний не подвергается метаболизму и элиминируется в основном с желчью и в меньшей степени - через почки. Длительность действия увеличивается у больных с печеночной недостаточностью, в то время как наличие почечной недостаточности не оказывает особого влияния на фармакокинети-ку препарата.
Дозировка
Мощность рокурония ниже мощности других сте-роидных миорелаксантов (мощность обратно пропорциональна скорости наступления эффекта). Доза, необходимая для проведения интубации, составляет 0,45-0,6 мг/кг. Для поддержания интра-операционной миорелаксации препарат вводят болюсом в дозе 0,15 мг/кг. Инфузионная доза варьируется от 5 до 12 мкг/(кг х мин). Длительность действия рокурония у больных в преклонном возрасте значительно увеличивается.
Побочные эффекты и особенности применения
Рокуроний (в дозе 0,9-1,2 мг/кг) - это единственный недеполяризующий миорелаксант, который начинает действовать так же быстро, как сукцинилхолин, что делает его препаратом выбора для быстрой последовательной индукции. Средняя продолжительность действия рокурония аналогична таковой векурония и атракурия. Рокуроний дает несколько более выраженный ваголитичес-кий эффект, чем панкуроний.
Случай из практики: замедленное пробуждение после общей анестезии
Мужчине, 72 лет, выполнили трансуретральную резекцию предстательной железы под общей анестезией. Через 20 мин после окончания операции у больного еще не восстановилось самостоятельное дыхание и сознание.
В чем состоит стандартный диагностический подход в этой ситуации?
Необходимо изучить анамнез, включая применяемые лекарственные средства, провести физикаль-ное и лабораторное исследования и проанализировать проведенную анестезию.
Какие заболевания увеличивают риск замедленного восстановления сознания и нервно-мышечной проводимости?
При артериальной гипертонии нарушается ауто-регуляция мозгового кровотока, что снижает толерантность головного мозга к эпизодам гипотонии. При болезнях печени снижается печеночный метаболизм лекарственных средств и их экскреция с желчью, что увеличивает продолжительность
Действия этих препаратов. Снижение концентрации альбумина в сыворотке крови увеличивает свободную (и, соответственно, активную) фракцию препарата. Печеночная энцефалопатия вызывает нарушения сознания. При болезнях почек нарушается экскреция многих лекарственных средств. Уремия тоже оказывает влияние на уровень сознания. Сахарный диабет сочетан с риском гипогликемии и гиперосмолярной гипергликемической неке-тоацидотической комы. Шумы над сонными артериями в сочетании с симптомами ишемии мозга, а также инсульт в анамнезе увеличивают риск развития интраоперационных нарушений мозгового кровообращения. Внутрисердечное шунтирование, особенно у детей с врожденными пороками сердца, может послужить причиной парадоксальной воздушной эмболии: пузырьки воздуха через дефекты поступают из венозной системы в артериальную, в том числе и в артерии головного мозга. Парадоксальная воздушная эмболия может вызвать необратимое повреждение мозга. Тяжелый гипотиреоз изменяет метаболизм лекарственных средств и, в редких случаях, вызывает микседема-тозную кому.
Насколько сужается диагностический поиск при наличии в анамнезе неосложненной предыдущей общей анестезии?
Неосложненная предыдущая общая анестезия, в ходе которой применяли сукцинилхолин, позволяет исключить врожденный дефект псевдохолинэстеразы. Снижение концентрации нормальной псевдохолинэстеразы не вызывает послеоперационного апноэ, за исключением чрезвычайно кратковременных вмешательств. Злокачественная ги-пертермия обычно не проявляется замедленным пробуждением, хотя и пролонгирует гипнотический эффект анестетиков. Неосложненная предыдущая общая анестезия не исключает злокачественной гипертермии. Замедленное пробуждение после анестезии в анамнезе может указывать на гиперчувствительность к анестетикам (например, у лиц преклонного возраста).
Могут ли лекарственные средства, принимаемые больным дома, повлиять на пробуждение?
Препараты, которые снижают МАК (например, резерпин или метилдопа), увеличивают риск передозировки анестетиков. Острое алкогольное отравление угнетает метаболизм барбитуратов и независимо от этого дает седативный эффект. Лекарственные средства, снижающие печеночный
Кровоток (например, циметидин), замедляют печеночный метаболизм. Препараты для лечения паркинсонизма и трициклические антидепрессанты, давая центральный антихолинергический эффект, потенцируют обусловленную скополами-ном седацию. Седативные средства длительного действия, например бензодиазепины, замедляют пробуждение.
Влияет ли методика анестезии на скорость пробуждения?
Методика премедикации может оказывать влияние на пробуждение. Особенно замедляет восстановление сознания в послеоперационном периоде использование холиноблокаторов (за исключением гликопирролата, который не проникает через гематоэнцефалический барьер), опиоидов и седа-тивных средств. Низкий сердечный выброс замедляет абсорбцию препарата при внутримышечном введении.
Методика поддержания анестезии тоже влияет на быстроту пробуждения. Использование комбинации закиси азота с опиоидами (например, с фен-танилом) сочетано с быстрым появлением ранних симптомов пробуждения, таких как открывание глаз или выполнение словесных инструкций. Однако скорость полного пробуждения приблизительно одинакова как для ингаляционной анестезии, так и для комбинации закиси азота с опиоидами.
Распространенной причиной послеоперационного апноэ является гипервентиляция во время операции. Так как ингаляционные анестетики повышают порог апноэ (так называют максимальное значение PaCO2, при котором больной еще не начинает дышать самостоятельно), то для стимуля-ции дыхательного центра целесообразна умеренная послеоперационная гиповентиляция. Тяжелая интраоперационная гипо- или гипертония увеличивают риск возникновения гипоксии и отека мозга.
Гипотермия снижает МАК, угнетает восстанов-ление нервно-мышечной проводимости и угнетает метаболизм лекарственных средств. Артериальная гипоксия и тяжелая гиперкапния (PaCO2 > 70 мм рт. ст.) вызывают нарушения сознания.
Некоторые оперативные вмешательства (например, каротидная эндартерэктомия, операции с искусственным кровообращением, операции на головном мозге) сочетаны с повышенным риском послеоперационного неврологического дефицита. После трансуретральной резекции предстательной железы часто возникает гипонатриемия разведения вследствие абсорбции ирригационного раствора.
Какие симптомы позволяет выявить физикальное исследование?
Диаметр зрачка не всегда служит адекватным показателем. Тем не менее если применение холиноблокаторов и ганглиоблокаторов (триметафана) исключено, то широкие фиксированные зрачки - угрожающий симптом. Реакция на болевой стимул (например, форсированное выдвижение нижней челюсти) позволяет отграничить угнетение сознания от миорелаксации. Тем же целям служит стимуляция периферического нерва.
Какие лабораторные и инструментальные методы исследования можно рекомендовать?
Целесообразно исследовать газы артериальной крови и электролиты сыворотки, особенно натрий. Консультант-невролог может назначить KT головного мозга.
Какое лечение следует назначить?
Необходимо продолжить ИВЛ. В зависимости от предполагаемой причины замедленного пробуждения применяют налоксон, флумазенил, физостигмин, доксапрам или аминофиллин.
Расслабление скелетных мышц может быть вызвано регионарной анестезией, высокими дозамиингаляционных анестетиков, а также препаратами, блокирующими нервно-мышечную передачу (их общепринятое название - миорелаксанты). В 1942 г. Гарольд Гриффит опубликовал результаты применения очищенного экстракта кураре (яда, которым южноамериканские индейцы смазывали наконечники стрел) при анестезии. Миорелаксанты быстро стали неотъемлемой частью лекарственного арсенала анестезиолога. Как отметил Гриффит, миорелаксанты вызывают расслабление скелетных мышц, а не анестезию.
N.B. Миорелаксанты не приводят к утрате сознания, амнезии и аналгезии.
Нервно-мышечная передача
Место, где мотонейрон вступает в контакт с мышечной клеткой, называется нервно-мышечным синапсом (см. рисунок). Клеточные мембраны мотонейрона и мышечной клетки разделены узким промежутком (20 нм) - синаптической щелью. Когда потенциал действия деполяризует терминаль мотонейрона, ионы кальция поступают извне в цитоплазму нерва, что вызывает слияниесинаптических пузырьков с пресинаптической терминальной мембраной и высвобождение содержащегося в них ацетилхолина в синаптическую щель.
Рисунок.
Молекулы ацетилхолина диффундируют через синаптическую щель и взаимодействуют сникотиночувствительными холинорецепторами (н-холинорецепторами) специализированной части мембраны мышечной клетки - концевой пластинкой скелетной мышцы.
Каждый холинорецептор состоит из пяти белковых субъединиц, две из которых (α-субъединицы) одинаковы и способны связывать молекулы ацетилхолина (одна α-субъединица - одно место связывания). Если оба места связывания заняты двумя молекулами ацетилхолина, то конформация субъединиц изменяется, что приводит к кратковременному (на 1 мс) открыванию ионного канала, проходящего через толщу рецептора (см. рисунок).
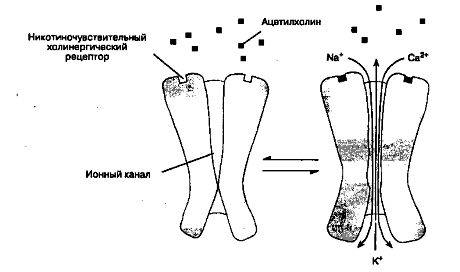
Рисунок . Связывание ацетилхолина с рецептором концевой пластинки скелетной мышцы приводит к открыванию канала и вызывает ионный ток
Через открытый канал начинают поступать катионы (натрий и кальций - извне внутрь клетки, калий - из клетки наружу), что вызывает появление потенциала концевой пластинки. Содержимое одного синаптического пузырька - квант ацетилхолина - вызывает миниатюрный потенциал концевой пластинки (1 квант - 10 000 молекул ацетилхолина). Если ацетилхолином занято достаточное количество рецепторов, то суммарный потенциал концевой пластинки становится достаточно мощным для того, чтобы деполяризовать постсинаптическую мембрану вокруг синапса. Натриевые каналы в этой части мембраны мышечной клетки открываются под воздействием разности потенциалов (в отличие от каналов в рецепторах концевой пластинки, которые открываются при взаимодействии с ацетилхолином). Возникающий потенциал действия распространяется вдоль мембраны мышечной клетки и системы Т-трубочек, что вызывает открывание натриевых каналов и выброс ионов кальция из цистерн саркоплазматической сети. Высвобожденный кальций опосредует взаимодействие сократительных белков актина и миозина, что приводит к сокращению мышечного волокна. Количество высвобожденного ацетилхолина обычно значительно превосходит минимум, необходимый для развития потенциала действия. Некоторые заболевания нарушают процесс нервно-мышечной передачи: при миастеническом синдроме Итона-Ламберта высвобождается недостаточное количество ацетилхолина, при миастении (myasthenia gravis ) снижено число холинорецепторов.
Субстратспецифический фермент ацетилхолинэстераза быстро гидролизует ацетилхолин на уксусную кислоту и холин. Молекулы этого фермента (называемого также специфической, илиистинной, холинэстеразой) фиксированы в концевой пластинке в непосредственной близости от холинорецепторов. В конечном счете ионные каналы закрываются, что приводит к реполяризации концевой пластинки. Когда распространение потенциала действия прекращается, ионные каналы в мембране мышечного волокна тоже закрываются. Кальций поступает обратно в саркоплазматическую сеть, и мышечное волокно расслабляется.
Деполяризующий и недеполяризующий блок
Миорелаксанты подразделяют на два класса: деполяризующие и недеполяризующие (см. таблицу). Это подразделение отражает различия в механизме действия, в реакции на стимуляцию периферического нерва и в последующем восстановлении нервно-мышечной проводимости.
| Деполяризующие миорелаксанты |
Недеполяризующие миорелаксанты |
| Короткого действия | Длительного действия |
| Сукцинилхолин | Тубокурарин |
| Декаметоний | Метокурин |
| Доксакурий | |
| Панкуроний | |
| Пипекуроний | |
| Галламин | |
| Средней продолжительности | |
| Атракурий | |
| Векуроний | |
| Рокуроний | |
| Короткого действия | |
| Мивакурий |
ТАБЛИЦА . Деполяризующие и недеполяризующие миорелаксанты
Механизм действия
Деполяризующие миорелаксанты, по структуре напоминающие ацетилхолин, взаимодействуют с н-холинорецепторами и вызывают потенциал действия мышечной клетки. Однако в отличие от ацетилхолина деполяризующие миорелаксанты не гидролизуются ацетилхолинэстеразой, и их концентрация в синаптической щели достаточно долго не снижается, что вызывает длительную деполяризацию конечной пластинки.
Длительная деполяризация конечной пластинки приводит к миорелаксации. Миорелаксация возникает следующим образом: как уже говорилось ранее, мощный потенциал концевой пластинки способен деполяризовать постсинаптическую мембрану вокруг синапса. Последующее открывание натриевых каналов, однако, носит кратковременный характер. После начального возбуждения и открывания каналы закрываются. Более того, натриевые каналы не могут снова открываться до тех пор, пока не произойдет реполяризация конечной пластинки. В свою очередь реполяризация конечной пластинки невозможна до тех пор, пока деполяризующий миорелаксант связан с холинорецепторами. Так как каналы в мембране вокруг синапса закрыты, потенциал действия иссякает и мембрана мышечной клетки реполяризуется, что и вызывает миорелаксацию. Такую блокаду нервно-мышечной проводимости принято называть I фазой деполяризующего блока.
Недеполяризующие миорелаксанты тоже связываются с холинорецепторами, но это не приводит к конформационным изменениям, вызывающим открывание канала. Так как при этом ацетилхолин не взаимодействует с рецепторами, то потенциал концевой пластинки не возникает.
N.B. Деполяризующие миорелаксанты действуют как агонисты холинорецепторов, а недеполяризующие - как конкурентные антагонисты.
Это основное различие в механизме действия объясняет разницу во влиянии препаратов на организм при некоторых заболеваниях. Например, хроническое снижение высвобождения ацетилхолина (при травматической денервации мышцы) стимулирует компенсаторное увеличение холинорецепторов на концевых пластинках скелетных мышц. Это потенцирует действие деполяризующих миорелаксантов (up-регуляция - деполяризуется больше рецепторов), но ослабляет эффект недеполяризующих миорелаксантов (необходимо блокировать больше рецепторов). Снижение числа холинорецепторов (например, down-регуляция при миастении), напротив, ослабляет действие деполяризующих миорелаксантов и потенцирует действие недеполяризующих.
Реакция на стимуляцию периферического нерва
Мониторинг нервно-мышечной передачи путем стимуляции периферического нерва и регистрации вызванного мышечного ответа обсуждался здесь. Для стимуляции используют электрические супрамаксимальные импульсы квадратной формы. Широко распространены четыре режима стимуляции.
Тетаническая стимуляция: непрерывная серия импульсов частотой 50-100 Гц, подаваемых в течение 5 с.
Одиночный стимул: одиночный импульс длительностью 0,2 mc.
Серия из четырех импульсов (английское название - train of four , сокращенно TOF ; в дальнейшем будет использоваться общепринятый термин « TOF -режим»): серия из четырех импульсов длительностью 0,2 mc каждый, подаваемых на протяжении 2 с (частота 2 Гц).
Стимуляция в режиме двойной вспышки (СРДВ): серия из трех коротких (0,2 mc) импульсов с интервалом 20 mc (частота 50 Гц), затем пауза длиной 750 mc, после чего повторяется два (СРДВ3,2) или три (СРДВ3,3) импульса, аналогичных начальным.
Затухание, т. е. постепенное снижение вызванного мышечного ответа при длительной или повторяющейся стимуляции нерва, характерно для действия недеполяризующих миорелаксантов. Затухание объясняется тем, что недеполяризующие миорелаксанты уменьшают количество доступного ацетилхолина, способного высвободиться при стимуляции нерва (блокада мобилизации ацетилхолина). Полноценное восстановление нервно-мышечной проводимости четко коррелирует с отсутствием затухания. Так как затухание лучше выявляется при тетанической стимуляции и при стимуляции в режиме двойной вспышки, чем при TOF-режиме и повторных одиночных стимулах, то именно первые два режима предпочтительно использовать для оценки полноценности восстановления нервно-мышечной проводимости в конце анестезии.
Способность тетанической стимуляции усиливать ответ на одиночный импульс получила названиепосттетанического облегчения . Посттетаническое облегчение может быть обусловлено компенсаторным увеличением мобилизации ацетилхолина после тетанической стимуляции.
В отличие от недеполяризующего блока для
- I фазы деполяризующего блока нехарактерно затухание при тетанической стимуляции и в TOF-режиме, не возникает и посттетанического облегчения. Однако, если доза деполяризующего миорелаксанта чрезмерно высока, качество блока изменяется - он начинает напоминать недеполяризующий.
- II фазы деполяризующего блока и может быть объяснен ионными и конформационными изменениями, возникающими при длительной деполяризации мышечной клетки.
Восстановление нервно-мышечной проводимости
N.B. Деполяризующие миорелаксанты не взаимодействуют с ацетилхолинэстеразой. Из области нервно-мышечного синапса они поступают в кровоток, после чего подвергаются гидролизу в плазме и печени под действием другого фермента - псевдохолинэстеразы (синонимы - неспецифическая холинэс-тераза, холинэстераза плазмы).
Этот процесс протекает очень быстро, что имеет благоприятный характер: специфические антидоты деполяризующего блока отсутствуют.
За исключением мивакуриума недеполяризующие миорелаксанты не гидролизуются ни ацетилхолинэстеразой, ни псевдохолинэстеразой. При недеполяризующем блоке восстановление нервно-мышечной проводимости обусловлено перераспределением, частичной метаболической деградацией и экскрецией недеполяризующих миорелаксантов или же может быть вызвано воздействием специфических антидотов - ингибиторов ацетилхолинэстеразы. Так как в нервно-мышечных синапсах ингибиторы ацетилхолинэстеразы увеличивают количество доступного ацетилхолина, конкурирующего с деполяризующими релаксантами, то они не способны устранять деполяризующий блок. В действительности, повышая концентрацию доступного ацетилхолина в нервно-мышечном синапсе и снижая активность псевдохолинэстеразы плазмы, ингибиторы ацетилхолинэстеразы увеличивают продолжительность деполяризующего блока.
Миорелаксанты вызывают расслабление скелетных мышц, что облегчает хирургический доступ и интубацию трахеи и позволяет ограничиться низкими дозами прочих анестетиков.
Одним из существенных рисков применения миорелаксантов, без адекватного количества наркотического или ингаляционного препарата, считается вероятность пребывания парализованного пациента во время в бодрствующем состоянии и в сознании. Последнее встречается крайне редко, но приводит к соответствующим психологическим и судебно-медицинским последствиям. Миорелаксанты на основании механизма действия подразделяют на деполяризующие и недеполяризующие средства.
Деполяризующие миорелаксанты
Для клинического применения в настоящее время доступен лишь один деполяризующий миорелаксант — сукцинилхолин (суксаметоний, дитилин). Характеризуется быстрым началом (15-30 с) и короткой продолжительностью действия (от 3 до 5 мин). У пациентов с «полным» желудком при проведении оперативного вмешательства сукцинилхолин часто используют для быстрой последовательной индукции (интраоперационное ведение).
Миорелаксант сукцинилхолин вызывает деполяризацию постсинаптической мембраны по механизму, напоминающему действие ацетилхолина. Препарат сначала вызывает временные мышечные сокращения, называемые фасцикуляциями, за которыми следует фаза расслабления. Данный миорелаксант метаболизируется холинэстеразой плазмы и не имеет специфического антагониста.
Побочные эффекты сукцинилхолина включают брадикардию (особенно у детей), гиперкалиемию, повышение внутриглазного и внутричерепного давления, злокачественную гипертермию (у подверженных субъектов) и послеоперационные миалгии. в мышцах шеи, плечах и брюшной стенки вызывают выраженную слабость, особенно в контексте .
Недеполяризующие миорелаксанты
Недеполяризующие релаксанты соединяются с нервно-мышечными рецепторами, за них они конкурируют с ацетилхолином, вызывающим активацию. Для релаксации скелетных мышц препарат должен занять более 70% рецепторов. Для начала действия может потребоваться несколько минут. Эффект данных препаратов устраняется соответствующими средствами.
На основании продолжительности эффекта миорелаксанты подразделяют на препараты короткого, промежуточного, длительного действия. Особое внимание к побочным влияниям на сердечно-сосудистую систему и различиям метаболизма позволяет для каждого пациента выбрать наиболее подходящее средство.
Миорелаксанты короткого действия. Мивакурий начинает действовать стремительно, метаболизируется холинэстеразой плазмы, и фармакологические антагонисты не требуются.
Мышечные релаксанты промежуточной длительности. К ним относятся атракурия безилат, цисатракурия безилат, векурония бромид, рокурония бромид. Для атракурия независимо от дозы характерна спонтанная деградация in vivo (элиминация Хоффмана), применение высоких доз сопровождается выделением гистамина. Цисатракурия безилат по свойствам аналогичен атракурия безилату, но для него характерно более медленное начало действия и минимальное высвобождение гистамина. Векурония бромид экскретируется почками и влияет на сердечно-сосудистую систему крайне незначительно. Рокурония бромид быстро начинает действовать и также минимально затрагивает гемодинамику. Предотвращение тахикардии и выраженной брадикардии имеет решающее значение у больных ИБС.
^ ПОБОЧНЫЕ ЭФФЕКТЫ 1. Аллергические реакции вплоть до анафилактических. 2. Наиболее часто встречаются мышечные боли после применения сукцинилхолина. Профилактика заключается в проведении прекураризации , т.е. введение за несколько минут до инъекции сукцинилхолина недеполяризующего миорелаксанта, хотя эта мера не всегда эффективна. Альтернативой прекураризации является внутривенное введение также за несколько минут до сукцинилхолина лидокаина. 3.Нарушения ритма сердца и артериальная гипотония Связано с высвобождением гистамина и ганглионарной блокадой. К резкой брадикардии и даже остановке сердца может привести гиперкалиемия в ответ на введение деполяризующих миорелаксантов при тяжелой травме, ожогах. 4.Длительное остаточное действие миорелаксантов при гиповолемии, нарушениях кровообращения, электролитных расстройствах и ацидозе может приводить к продленному апноэ. 5. Регургитация и аспирация желудочного содержимого в трахеобронхиальное дерево у больных с "полным" желудком. С целью профилактики рекомендуется опорожнить желудок с помощью зонда, обеспечить возвышенное положение головы и туловища. Кроме того, рекомендуют в премедикации использовать препараты, уменьшающие желудочную секрецию (например, блокаторы H 2 -гистаминовых рецепторов). 6.Злокачественная гипертермия - самое опасное осложнение, встречаемое при использовании сукцинилхолина. Злокачественная гипертермия - функциональные нарушения обмена кальция при патологических отклонения в физиологии мышц, хотя повреждаются при этом и другие структуры, связанные с кальцием (миокард, нервы, тромбоциты, лимфоциты и др.). Синдром может развиться как во время вводной анестезии, так и спустя несколько часов после ее окончания. Самые частые триггеры - сукцинилхолин и галотан, хотя ими могут быть и другие препараты (калипсол, лидокаин и др.). Злокачественная гипертермия может усиливаться адреналином, сердечными гликозидами, солями кальция, дериватами теофиллина. Пипекуроний (ардуан) Препарат не вызывает высвобождение гистамина и не влияет на кровообращение При введении 0,07 мг/кг оптимальные условия для интубации возникают через 3 мин, а клинически эффективный блок длится 70 мин. Панкуроний (павулон) Отличительной особенностью препарата является его способность блокировать влияние вагуса и высвобождать катехоламины из адренергических нервных окончаний, а также ингибировать реаптейк норадреналина. В связи с этим побочными эффектами препарата являются тахикардия, умеренная гипертензия, аритмии, повышение потребности миокарда в кислороде Наиболее часто применяются в практике: дитилин, ардуан, диплацин
Мышечные релаксанты - это препараты, которые расслабляют поперечно-полосатую мускулатуру.
Из этой статьи вы узнаете классификацию мышечных релаксантов, а также о том, как действуют мышечные релаксанты в анестезиологии.
Действие мышечных релаксантов
Как используют мышечные релаксанты препараты?
Прежде всего, они используются для эндотрахеальной интубации. Очень важным эффектом мышечных релаксантов является предотвращение рефлекторной активности всей произвольной мускулатуры. Во время анестезии без применения миорелаксантов мышцы сохраняют достаточный тонус, который может затруднять действия хирурга. Кроме того, использование мышечных релаксантов позволяет анестезиологу проводить наркоз, применяя меньшие дозы анестетиков, что, естественно снижает риск анестезии.
Очень важно, что эти препараты, вызывая полную нейромышечную блокаду, резко уменьшают патологическую импульсацию, идущую от мышц в центральную нервную систему. Следовательно, миорелаксация помогает, наряду с другими компонентами общей анестезии, добиться эффективной защиты больного от операционного стресса.
Кроме того, мышечные релаксанты применяют для предотвращения спазмов мускулатуры при таких заболеваниях, как столбняк, бешенство, эпилептический статус и некупирующиеся судороги любой этиологии.
Классификация мышечных релаксантов
Хорошо известно, что все мышечные релаксанты разделяются на две большие группы в зависимости от механизма их действия: деполяризующие и недеполяризующие (конкурентные). Для того чтобы представить себе механизм их действия, необходимо кратко рассмотреть физиологию нейромышечной передачи.
Физиология нейромышечной передачи
Каждая веточка двигательного нерва заканчивается нервномышечным синапсом. Он представляет собой две мембраны: мембрана нервного окончания (пресинаптическая) и мембрана мышечного волокна (постсинаптическая или моторная концевая пластинка). Между мембранами имеется синаптическая щель размером около 500 ангстрем, заполненная жидкостью с консистенцией геля. Передача импульса с нерва на мышечное волокно осуществляется за счет выделения ацетилхолина, который синтезируется и хранится в пресинаптическом окончании.
В состоянии покоя моторная концевая пластинка находится в поляризованном состоянии - отрицательный электрический заряд на внутренней, а положительный - на наружной поверхности мембраны.
При раздражении двигательного нерва выделяется ацетилхолин, который проходит через пресинаптическую мембрану и вливается в синаптическую щель. Там он взаимодействует с холинергическими рецепторами моторной концевой пластинки.
При соединении ацетилхолина с рецепторами наблюдается резкое изменение проницаемости постсинаптической мембраны, прежде всего для ионов натрия и калия. Результатом этого является деполяризация моторной концевой пластины и возникновение на ней локального потенциала, за которым следует сокращение мышечного волокна.
Ацетилхолин в течение миллисекунд после связывания с холинэргическими рецепторами прекращает свое действие под влиянием холинэстеразы, которая разлагает его на холин и уксусную кислоту. В результате этого постсинаптическая мембрана реполяризуется, а мышечное волокно расслабляется.
Деполяризующие и недеполяризующие миорелаксанты
Механизм действия недеполяризующих мышечных релаксантов заключается в том, что они имеют сродство к ацетилхолиновым рецепторам и конкурируют с ацетилхолином за возможность связывания с ними, препятствуя доступу медиатора к рецепторам. В результате воздействия конкурентных нейромышечных блокаторов постсинаптическая мембрана оказывается в состоянии стойкой поляризации и теряет способность к деполяризации. Соответственно, мышечное волокно теряет способность к сокращению.
Нейромышечную блокаду вызванную недеполяризующими миорелаксантами можно прекратить с помощью введения антихолинэстеразных препаратов (прозерин, неостигмин, галантамин). Они способны блокировать холинэстеразу и, тем самым, предотвращать разрушение ацетилхолина. При этом конкуренция за рецепторы постсинаптической мембраны сдвигается в сторону естественного медиатора и нервномышечная проводимость восстанавливается.
Миопарализующий эффект деполяризующих миорелаксантов связан с тем, что они действуют на постсинаптическую мембрану подобно ацетилхолину, деполяризуя ее и вызывая стимуляцию мышечного волокна. Однако, вследствие того, что они не удаляются немедленно с рецептора и блокируют доступ к нему ацетилхолина, деполяризация оказывается относительно длительной и недостаточной для сохранения мышцы в сокращенном состоянии. Поэтому последняя расслабляется.
Естественно, что использование антихолинэстеразных препаратов в качестве антидотов деполяризующих миорелаксантов будет неэффективным, так как накапливающийся при этом ацетилхолин будет только усиливать деполяризацию концевой мембраны и, следовательно, усиливать, а не уменьшать, степень нейромышечной блокады.
Вторая фаза действия релаксантов
Интересно, что во всех случаях даже однократного введения деполяризующих миорелаксантов, не говоря уже о введении повторных доз, на постсинаптической мембране обнаруживаются изменения той или иной степени выраженности, заключающиеся в том, что деполяризующая блокада сопровождается блокадой недеполяризующего типа. Это так называемая вторая фаза действия (более ранний термин - "двойной блок") данного типа мышечных релаксантов. Механизм второй фазы действия до сих пор неизвестен. Очевидно, что вторая фаза действия может в последующем устраняться антихолинэстеразными препаратами и усиливаться недеполяризующими мышечными релаксантами.
