Farmakoloogilised omadused
Praegu toodetakse palju mittedepolariseerivaid ravimeid (tabel 9-6). Mittedepolariseeriva lihasrelaksandi valik sõltub ravimi individuaalsetest omadustest, mille määrab suuresti selle struktuur. Näiteks steroidühenditel on vagolüütiline toime (see tähendab, et nad pärsivad vaguse närvi funktsiooni) ja bensokinoliinid vabastavad nuumrakkudest histamiini.
A. Mõju autonoomsele närvisüsteemile. Mittedepolariseerivatel lihasrelaksantidel kliinilistes annustes on erinev toime n- ja m-kolinergilistele retseptoritele. Tubokurariin ja vähemal määral metokuriin blokeerivad autonoomseid ganglioneid, mis nõrgendavad sümpaatilise närvisüsteemi poolt vahendatud südame löögisageduse ja müokardi kontraktiilsuse tõusu arteriaalse hüpotensiooni ja muud tüüpi operatsioonistressi korral. Pankuroonium ja gal-lamiin, vastupidi, blokeerivad sinoatriaalse sõlme m-kolinergilisi retseptoreid, mis põhjustab tahhükardiat.
TABEL 9-6. Mittedepolariseerivate lihasrelaksantide farmakoloogia
Märge. Toime algus: + - aeglane; ++ - mõõdukalt kiire; +++ - kiire.
Toime kestus: + - lühitoimeline ravim; ++ - keskmise toimeajaga ravim;
Pikatoimeline ravim.
Histamiini vabanemine: O - puudub; + - ebaoluline; ++ - keskmine intensiivsus; +++ – märkimisväärne.
Vagusnärvi blokaad: O - puudub; + - ebaoluline; ++ - keskmine.
2 Põhineb 1 ml ravimi keskmisel hulgihinnal, mis ei kajasta kõigil juhtudel toime tugevust ja kestust.
Gallamiini võimas vagolüütiline toime (piiratud südame kolinergiliste retseptoritega. – Märkus trans.) Kitsendas oluliselt selle kliinilist kasutamist. Soovitatavates annustes kasutamisel ei avalda atrakuurium, mivakuuria, doksakuurium, vekuranium ja pipcuronium olulist mõju autonoomsele närvisüsteemile.
B. Histamiini vabanemine. Histamiini vabanemine nuumrakkudest võib perifeerse vasodilatatsiooni tõttu põhjustada bronhospasmi, naha punetust ja hüpotensiooni. Histamiini vabanemise vähenemine on esitatud järgmiselt: tubo-kurariin> metokuriin> atrakuurium ja mivakuurium. Aeglane manustamiskiirus ja H1- ja H2-blokaatorite eelnev kasutamine kõrvaldavad need kõrvaltoimed.
B. Maksa kliirens. Maksas metaboliseeruvad ulatuslikult ainult pankuroonium ja vekuroonium. Peamine vekuraani ja rokurooniumi eritumistee on sapi kaudu. Maksapuudulikkus pikendab pankurooniumi ja rokurooniumi toimet, kuid mõjub vekurooniumile nõrgemalt. Atrakuurium ja mivakuurium läbivad intensiivse ekstrahepaatilise metabolismi.
D. Eritumine neerude kaudu. Metokuriini ja gallamiini eliminatsioon sõltub peaaegu täielikult neerude eritumisest, mistõttu on need ravimid neerupuudulikkuse korral vastunäidustatud. Metokuriin ja gallamiin on aga ioniseeritud, nii et neid saab hemodialüüsi abil eemaldada. Tubokurariin, doksakuurium, pankuroonium, vekuroonium ja pipkuroonium erituvad neerude kaudu vaid osaliselt, mistõttu neerupuudulikkus pikendab nende toimet. Atrakuuria ja mivakuria eliminatsioon ei sõltu neerufunktsioonist.
E. Hingetoru intubatsiooni kasutamise võimalus. Ainult rokuroon kutsub esile neuromuskulaarse blokeerimise sama kiiresti kui suktsinüülkoliin. Mittedepolariseerivate lihasrelaksantide toime kujunemist saab kiirendada nende suurte või küllastavate annuste kasutamisel. Kuigi suur annus kiirendab lihaste lõõgastumise algust, süvendab see samal ajal kõrvaltoimeid ja pikendab toimeaega. Näiteks pankurooniumi manustamisel annuses 0,15 mg / kg on hingetoru intubeerimine võimalik 90 sekundi pärast, kuid sel juhul tekib raske arteriaalne hüpertensioon ja tahhükardia ning pöördumatu blokaadi kestus võib ületada 45 minutit. .
Keskmise kestusega ravimite (atrakuurium, vekuroonium, rokuroonium) ja lühitoimeliste ravimite (mivakuurium) ilmumine tõi kaasa lihasrelaksantide laialdase kasutuselevõtu kahes annuses, kasutades küllastavat annust. Teoreetiliselt põhjustab 10–15% standardsest intubatsiooniannusest manustamine 5 minutit enne anesteesia esilekutsumist märkimisväärse hulga n-kolinergiliste retseptorite blokeerimist, nii et ülejäänud annuse järgneval süstimisel toimub lihaste lõdvestumine kiiresti. Küllastav annus ei põhjusta tavaliselt kliiniliselt olulist skeletilihaste halvatust, kuna see nõuab 75–80% retseptorite blokeerimist (neuromuskulaarne ohutusvaru). Kuid mõnel juhul blokeerib küllastusannus piisavalt suur number retseptorid, mis põhjustab õhupuudust ja düsfaagiat. Sel juhul tuleb patsienti rahustada ja kiiresti anesteesia esile kutsuda. Hingamispuudulikkuse korral võib küllastav annus oluliselt kahjustada hingamisfunktsiooni ja vähendada oksühemoglobiini kogust. Küllastusdoos võimaldab hingetoru intubeerida 60 s pärast rokurooniumi põhidoosi ja 90 s pärast ülejäänud keskmise toimeajaga lihasrelaksantide põhidoosi manustamist. Rokuroonium on mittedepolariseeriv lihasrelaksant, mis on valitud kiireks järjestikuseks induktsiooniks, kuna see kutsub kiiresti esile lihaste lõdvestamise, ei too kaasa olulisi kõrvaltoimeid isegi suurtes annustes kasutamisel ja sellel on mõõdukas toimeaeg.
E. Lummustused. Fastikulatsioonide vältimiseks manustatakse 5 minutit enne suktsinüülkoliini intubatsiooniks (prekurariseerimiseks) 10-15% mittedepolariseeriva lihasrelaksanti standardannusest. Sel eesmärgil saab kasutada valdavat enamust mittedepolariseerivatest lihasrelaksante, millest tõhusaim on tubo-kurariin. Kuna mittedepolariseerivad lihasrelaksandid on depolariseeriva ploki I faasi antagonistid, peaks suktsinüülkoliini annus olema suur (1,5 mg / kg).
G. Inhaleeritavate anesteetikumide võimendav toime. Inhalatsioonianesteetikumid vähendavad mittedepolariseerivate lihasrelaksantide vajadust vähemalt 15%. Postsünaptilise võimendamise aste sõltub nii kasutatavast anesteetikumist (isofluraan, sevofluraan, desfluraan ja enfluraan> halotaan> dilämmastikoksiid / hapnik / opiaat) kui ka kasutatavast lihasrelaksandist (tubokurariin ja pankuroonium> vekuroonium ja atrakuurium).
3. Teiste mittedepolariseerivate lihasrelaksantide võimendav toime: mõnede mittedepolariseerivate lihasrelaksantide (näiteks tubokurariin ja pankuroonium) kombinatsioon ei põhjusta mitte aditiivset, vaid võimendavat toimet. Mõnede kombinatsioonide täiendav eelis on
Kõrvaltoimed vähenevad: näiteks pankuroonium nõrgendab tu-bokurariini hüpotensiivset toimet. Sarnase struktuuriga lihasrelaksantide (näiteks vekuroonium ja pankuroonium) koostoime võimetuse puudumine tekitas teooria, et võimendamine toimub toimemehhanismi väikeste erinevuste tagajärjel.
Mõnede parameetrite mõju mittedepolariseerivate lihasrelaksantide farmakoloogilistele omadustele
Temperatuur. Hüpotermia pikendab neuromuskulaarset blokaadi metabolismi pärssimise (nt mivakuuria, atrakuurium) ja aeglustunud eritumise (nt tubokurariin, metokuriin, pankuroonium) tõttu.
B. Happe-aluse tasakaal. Respiratoorne atsidoos võimendab enamiku mittedepolariseerivate lihasrelaksantide toimet ja pärsib neuromuskulaarse juhtivuse taastumist atsetüülkoliinesteraasi inhibiitoritega. Järelikult takistab hüpoventilatsioon operatsioonijärgsel perioodil neuromuskulaarse juhtivuse täielikku taastumist. Teave muude happe-aluse tasakaaluhäirete mõju kohta on vastuoluline, kuna kaasnevad muutused rakuvälise vedeliku pH-s, rakusisese pH-s, elektrolüütide kontsentratsioonis ja lihasrelaksantide (nt mono- ja bis-kvaternaarsed ammooniumiühendid) struktuurierinevused; steroidsed lõõgastajad ja bensokinoliinid).
B. Elektrolüütide häired. Hüpokaleemia ja hüpokaltseemia võimendavad mittedepolariseerivat blokaadi. Hüperkaltseemia tagajärjed on ettearvamatud. Hüpermagneseemia, mis võib tekkida preeklampsia ravimisel magneesiumsulfaadiga, võimendab mittedepolariseerivat blokaadi, konkureerides kaltsiumiga skeletilihaste otsaplaatides.
D. Vanus. Vastsündinutel on neuromuskulaarsete sünapside ebaküpsuse tõttu suurenenud tundlikkus lihasrelaksantide suhtes. See ülitundlikkus ei pruugi aga põhjustada lihasrelaksantide vajaduse vähenemist – vastsündinute suur rakuväline ruum suurendab jaotusmahtu.
D. Koostoime ravimitega. Nagu märgitud, võimendavad paljud ravimid mittedepolariseerivat blokaadi (tabel 9-4). Koostoimed toimuvad erinevatel tasanditel: presünaptilised struktuurid, postsünaptilised kolinergilised retseptorid ja lihasraku membraanid.
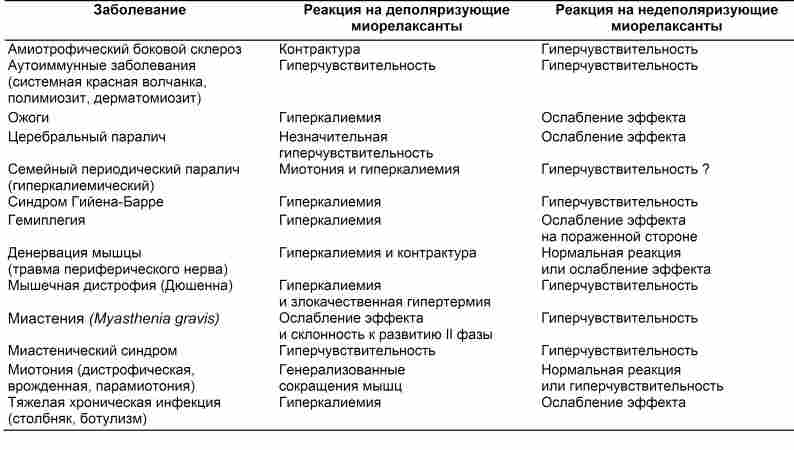
E. Kaasuvad haigused. Närvisüsteemi ja lihaste haigused avaldavad lihasrelaksantide toimele tugevat mõju (tabelid 9-7). Maksatsirroos ja krooniline neerupuudulikkus suurendavad sageli vees lahustuvate ravimite, nagu lihasrelaksandid, jaotusmahtu ja vähendavad plasmakontsentratsiooni. Samal ajal pikeneb ravimite toimeaeg, mille metabolism sõltub eritumisest maksa ja neerude kaudu. Seega on maksatsirroosi ja kroonilise neerupuudulikkuse korral soovitatav kasutada lihasrelaksandi suuremat algannust (koormus) ja väiksemat säilitusannust (võrreldes standardtingimustega).
G. Erinevate lihasrühmade reaktsioon. Lihaslõõgastuse algus ja selle kestus on erinevates lihasrühmades väga erinev. See varieeruvus võib olla tingitud ebaühtlasest verevoolust, erinevatest kaugustest suurte veresoonteni ja ebaühtlasest kiu koostisest. Lisaks erineb erinevate lihasrelaksantide kasutamisel lihasrühmade suhteline tundlikkus. Mittedepolariseerivate lihasrelaksantide kasutuselevõtuga diafragmasse, kõri lihastesse ja silma ringlihasesse toimub lihaste lõdvestumine ja kaob kiiremini kui lihastes. pöial pintslid. Sel juhul võib diafragma kokku tõmbuda isegi siis, kui pöidla röövimislihas ei reageeri ulnaarnärvi stimulatsioonile (täiendava ohutuse tagamisena desorienteerib see omadus anestesioloogi). Glottise lihased võivad olla vastupidavad lihasrelaksantide toimele, mida sageli täheldatakse larüngoskoopiaga.
Lihaslõõgastuse kestust ja sügavust mõjutavad paljud tegurid, seetõttu on lihasrelaksantide toime hindamiseks vajalik jälgida neuromuskulaarset juhtivust. Soovitatavad annused, sealhulgas selles peatükis toodud, on soovituslikud ja vajavad korrigeerimist sõltuvalt individuaalsest tundlikkusest.
Tubokurariin
Struktuur
Tubokurariin (d-tubokurariin) on monokvaternaarne ammooniumiühend, mis sisaldab tertsiaarset aminorühma (joonis 9-3). Kvaternaarne ammooniumirühm jäljendab atsetüülkoliini molekuli positiivselt laetud osa ja vastutab seetõttu retseptoriga seondumise eest, samas kui tubokurariini molekuli suur rõngakujuline osa häirib retseptori stimuleerimist.
TABEL 9-7. Haigused, mille puhul reaktsioon lihasrelaksantidele muutub
Ainevahetus ja eritumine
Tubokurariin ei metaboliseeru oluliselt. Eritumine toimub peamiselt neerude kaudu (50% ravimist eritub esimese 24 tunni jooksul) ja vähemal määral sapiga (10%). Neerupuudulikkuse esinemine pikendab ravimi toimet.
Annustamine
Intubatsiooniks vajalik tubokurariini annus on 0,5-0,6 mg/kg, seda manustatakse aeglaselt 3 minuti jooksul. Operatsioonisisene lõõgastus saavutatakse laadimisannusega 0,15 mg / kg, mis asendatakse fraktsioneeriva manustamisega 0,05 mg / kg. Kehakaaluga 70 kg vastab see küllastusannusele 9 mg, seejärel manustatakse 3 mg ravimit iga 20-30 minuti järel.
Lastel ei ole küllastusdoosi vajadus väiksem, samas kui ravimi säilitusannuste manustamise vahelised intervallid on pikemad. Vastsündinute tundlikkus tubokurariini suhtes on märkimisväärne
Varieerub. Tubokurariini vabaneb 3 mg 1 ml lahuses. Hoida toatemperatuuril.
A. Arteriaalne hüpotensioon ja tahhükardia. Need tekivad peamiselt histamiini vabanemise tõttu. Tubokurariini mõju autonoomsetele ganglionidele mängib teisejärgulist rolli.
B. Bronhospasm. See on tingitud histamiini vabanemisest. Tubokurariini ei tohi kasutada bronhiaalastma raviks.
Metokurin
Struktuur
Metokuriin on tubokurariini bis-kvaternaarne derivaat, mida nimetatakse ka dimetüültubokurariiniks. Tubokurariini ja metokuriini paljude farmakoloogiliste omaduste ja kõrvaltoimete sarnasus on tingitud struktuurilisest analoogiast.
Ainevahetus ja eritumine
Sarnaselt tubokurariiniga ei metaboliseeru metokuriin ja see eritub peamiselt läbi
Neerud (50% ravimist esimese 24 tunni jooksul). Neerupuudulikkuse esinemine pikendab ravimi toimet. Sapi eritumisel on tähtsusetu roll (
Annustamine
Intubatsioon on võimalik ravimi manustamisel annuses 0,3 mg / kg. Aeglane manustamine 1-2 minuti jooksul vähendab kõrvaltoimeid. Intraoperatiivse lihaslõõgastuse laadimisannus on 0,08 mg / kg, säilitusannus on 0,03 mg / kg.
Tubokurariini pediaatrias kasutamise iseärasused kehtivad ka metokuriini kasutamise kohta. Olenemata vanusest on metokuriini tugevus 2 korda suurem kui tubokurariinil.
Kõrvaltoimed ja rakenduse omadused
Metokuriini manustamine tubokurariini annustega võrdsetes annustes põhjustab poole histamiini kogusest vabanemise. Sellegipoolest tekivad suurte annuste kasutamisel arteriaalne hüpotensioon, tahhükardia, bronhospasm ja allergilised reaktsioonid. Joodiallergia (mis tekib nt kalaallergiaga) on kasutamise vastunäidustuseks, kuna ravim sisaldab joodi.
Atrakuuriumi struktuur
Atrakuuriumi koostis, mis on tüüpiline kõigile lihasrelaksantidele, sisaldab kvaternaarset ammooniumirühma. Samal ajal tagab atrakuuriumi bensokinoliini struktuur ravimi metabolismi.
Ainevahetus ja eritumine
Atrakuuriumi metabolism on nii intensiivne, et selle farmakokineetika ei sõltu maksa- ja neerufunktsiooni seisundist: vähem kui 10% ravimist eritub muutumatul kujul uriini ja sapiga. Ainevahetust tagavad kaks sõltumatut protsessi.
A. Eetersideme hüdrolüüs. Seda protsessi katalüüsivad mittespetsiifilised esteraasid ning atsetüülkoliinesteraas ja pseudokoliinesteraas ei ole sellega seotud.
B. Hoffmani kõrvaldamine. Füsioloogilise pH ja kehatemperatuuri juures toimub atrakuurium spontaanse mitteensümaatilise keemilise hävitamise.
Annustamine
Intubatsiooniks vajalik annus on 0,5 mg/kg, see manustatakse 30-60 sekundi jooksul. Intraoperatiivse lihaslõõgastuse laadimisannus on 0,25 mg / kg, säilitusannus on 0,1 mg / kg iga 10-20 minuti järel. Infusioon annuses 5-10 mcg / (kg x min) asendab täielikult fraktsionaalset manustamist.
Kuigi vajadus ravimi järele sõltub patsiendi vanusest vähe, on atrakuuriumi toimeaeg lastel siiski lühem kui täiskasvanutel.
Atrakuurium vabaneb lahuste kujul, mis sisaldavad 10 mg 1 ml-s. Ravimit tuleb hoida külmkapis temperatuuril 2-8 0C, kuna iga kuu toatemperatuuril hoidmine vähendab selle võimsust 5-10%.
Kõrvaltoimed ja kliiniline kasutamine
Võrreldes tubokurariini ja metokuriiniga vabastab atrakuurium histamiini vähemal määral.
A. Arteriaalne hüpotensioon ja tahhükardia. Vereringesüsteemiga seotud kõrvaltoimed on haruldased, tingimusel et ravimi annus ei ületa 0,5 mg / kg. Atrakuurium on samuti võimeline põhjustama mööduvat TPRV langust ja südameindeksi tõusu, sõltumata histamiini vabanemisest. Aeglane süstimiskiirus vähendab neid kõrvaltoimeid.
B. Bronhospasm. Atrakuuriumi ei tohi kasutada bronhiaalastma korral. Lisaks võib atrakuurium põhjustada tõsist bronhospasmi, isegi kui bronhiaalastmat pole varem esinenud.
B. Laudanosiini toksilisus. Laudanosiin on atrakuuriumi metabolismi produkt, mis moodustub Hoffmani eliminatsiooni käigus. Laudanosiin stimuleerib kesknärvisüsteemi, mis suurendab vajadust anesteetikumide järele (suurendab MAC-i) ja kutsub isegi esile krampe. Nende mõjude raskusaste ei saavuta valdaval enamusel juhtudest kliinilist tähtsust; erandid ilmnevad ravimi liiga suure koguannuse kasutamisel või maksapuudulikkuse korral (laudanosiin metaboliseerub maksas).
D. Tundlikkus kehatemperatuuri ja pH suhtes. Hüpotermia ja atsidoos pärsivad Hoffmani eliminatsiooni, mis pikendab atrakuuriumi toimet.
D. Keemiline kokkusobimatus. Kui atrakuurium sisestatakse leeliselist lahust (näiteks tiopentaali) sisaldavasse intravenoossesse infusioonisüsteemi, sadestub see happena.
Tsisatrakuuriumi struktuur
Tsisatrakuurium on uus mittedepolariseeriv lõõgastav aine, mis on atrakuuriumi isomeer. Selle ravimi katsed on praegu käimas.
Ainevahetus ja eritumine
Füsioloogilise pH ja kehatemperatuuri juures läbib tsisatrakuurium, nagu ka atrakuurium, Hoffmani eliminatsiooni. Selle reaktsiooni tulemusena tekivad metaboliidid (monokvaternaarne akrülaat ja laudanosiin), mis ei põhjusta neuromuskulaarset blokaadi. Mittespetsiifilised esteraasid ei osale tsisatrakuuriumi metabolismis. Neeru- ja maksapuudulikkus ei mõjuta tsisatrakuuria metabolismi ega eliminatsiooni.
Annustamine
Intubatsiooni annus on 0,1-0,15 mg / kg, seda manustatakse 2 minuti jooksul, mis põhjustab keskmise kestusega neuromuskulaarse blokaadi. Infusioon annuses 1-2 μg / (kg x min) võimaldab säilitada operatsioonisisese lihaslõõgastuse. Seega on Cisatracurium sama efektiivne kui Vecuronium.
Tsisatrakuriumi tuleb hoida külmkapis temperatuuril 2–8 ° C. Kui ravim on külmkapist välja võetud ja toatemperatuuril hoitud, tuleb see ära kasutada 21 päeva jooksul.
Kõrvaltoimed ja rakenduse omadused
Tsisatrakuurium, erinevalt atrakuuriumist, ei põhjusta plasma histamiini taseme püsivat annusest sõltuvat tõusu. Tsisatrakuurium ei mõjuta südame löögisagedust, vererõhku ega autonoomset närvisüsteemi isegi LD 95-st 8 korda suurema annuse korral.
Laudanosiini toksilisus, tundlikkus kehatemperatuuri ja pH suhtes ning atrakuuriale iseloomulik keemiline kokkusobimatus on tsisatrakuuria puhul võrdselt levinud.
Mivakuuriumi struktuur
Mivakuurium on bensokinoliini derivaat.
Ainevahetus ja eritumine
Mivakuurium, nagu suktsinüülkoliin, hüdrolüüsitakse pseudokoliinesteraasi toimel. Tõeline koliinesteraas osaleb mivakuuria metabolismis äärmiselt vähe. Järelikult, kui pseudokoliinesteraasi kontsentratsioon väheneb (tabel 9-3) või see on esindatud ebatüüpilise variandiga, pikeneb mivakuuria toime kestus oluliselt. Heterosügootse defektse pseudokoliinesteraasi geeniga kestab blokaad 2-3 korda kauem kui tavaliselt, homosügootse korral - võib püsida tunde. Kuna homosügootse defekti korral ei metaboliseeri pseudokoliinesteraas mivakuuriat, muutub neuromuskulaarse blokaadi kestus sarnaseks pikatoimeliste lihasrelaksantide manustamisega. Vastupidiselt suktsinüülkoliinile kõrvaldavad atsetüülkoliinesteraasi inhibiitorid mivakuuria müoparalüütilise toime vähemalt nõrga lihaste reaktsiooni juuresolekul närvistimulatsioonile. Hoolimata asjaolust, et mivakuuria metabolism ei sõltu otseselt maksa- või neerufunktsiooni seisundist, pikeneb selle toime kestus maksa- või neerupuudulikkuse korral pseudokoliinesteraasi kontsentratsiooni vähenemise tõttu plasmas.
Annustamine
Intubatsiooniks vajalik annus on 0,15-0,2 mg / kg. Infusioon algannusega 4-10 μg / (kg x min) võimaldab lihaseid lõdvestada operatsiooni ajal. Täpne annus sõltub pseudokoliinesteraasi plasmakontsentratsioonist. Kehakaalu järgi vajavad lapsed suuremaid ravimiannuseid kui täiskasvanud (kehapinna järgi on annused samad).
Kõrvaltoimed ja rakenduse omadused
Mivakuurium vabastab histamiini kvantitatiivselt sarnaselt atrakuuriumiga. Ravimi aeglane manustamine (1 minuti jooksul) vähendab histamiini vabanemisest põhjustatud arteriaalset hüpotensiooni ja tahhükardiat. Sellegipoolest, kui mivakuuria annus ületab 0,15 mg / kg, ei hoia isegi ravimi aeglane manustamine südamehaiguste korral ära vererõhu järsku langust. Mivakuria toime algus on sarnane atrakuuriaga (2-3 minutit). Mivakuuria peamiseks eeliseks on selle lühike toimeaeg (20-30 minutit), mis on 2-3 korda pikem kui suktsinüülkoliini ploki I faas, kuid 2 korda lühem kui atrakuuriumi, vekurooniumi ja rokurooniumi toime kestus. Lastel hakkab ravim toimima kiiremini ja toimeaeg on lühem kui täiskasvanutel. Mivacurium säilib toatemperatuuril 18 kuud.
Doksakuurium
Struktuur
Doksakuurium on bensokinoliiniühend, mis meenutab struktuurilt mivaakuuriumi ja atrakuuriumi.
Ainevahetus ja eritumine
Seda võimsat pikatoimelist lihasrelaksanti hüdrolüüsib plasma koliinesteraas vaid vähesel määral. Nagu ka teiste pikatoimeliste lihasrelaksantide puhul, on eliminatsiooni peamine tee neerude kaudu. Neeruhaiguse korral pikeneb doksakuuria toime kestus. Sapi eritumine ei mängi doksakuuria eliminatsioonis olulist rolli.
Annustamine
Intubatsiooniks vajalik annus on 0,05 mg/kg. Intubatsiooni võib läbi viia 5 minutit pärast manustamist. Intraoperatiivse lihaste lõdvestamise laadimisannus on 0,02 mg / kg, säilitusannused on 0,005 mg / kg. Doksakuuria annused lastel ja eakatel on kehakaalu poolest sarnased ülalmainitutega, kuigi vanemas eas kestab doksakuuria kauem.
Kõrvaltoimed ja rakenduse omadused
Doxacuria ei vabasta histamiini ega mõjuta vereringet. See hakkab toimima veidi aeglasemalt kui teised pikatoimelised mittedepolariseerivad lihasrelaksandid (4-6 minuti pärast), samas kui toime kestus on sarnane pankurooniumi omaga (60-90 minutit).
Pankuroonium
Struktuur
Pankuroonium koosneb steroiditsüklist, mille külge on kinnitatud kaks modifitseeritud atsetüülkoliini molekuli (bis-kvaternaarne ammooniumiühend). Pankuroonium seondub kolinergilise retseptoriga, kuid ei stimuleeri seda.
Ainevahetus ja eritumine
Erinevalt tubokurariinist ja metokuriinist metaboliseerub pankuroonium teatud määral maksas (desatsetüülimine). Ainevahetusproduktil on ka müoparalüütiline toime. Eritumine toimub peamiselt neerude kaudu (40%), vähemal määral sapiga (10%). Loomulikult aeglustub neerupuudulikkuse korral pankurooniumi eliminatsioon ja pikeneb neuromuskulaarne blokaad. Suurenenud jaotusmahust tingitud maksatsirroosi korral on vaja algannust suurendada, kuid säilitusannust vähendatakse madala kliirensi tõttu.
Annustamine
Pankurooniumi jõud on poole väiksem kui doksakuuriumil. 2–3 minuti jooksul pärast pankurooniumi manustamist annuses 0,08–0,12 mg / kg saab hingetoru intubeerida. Intraoperatiivse lihaslõõgastuse laadimisannus on 0,04 mg / kg, säilitusannus on 0,01 mg / kg iga 20-40 minuti järel.
Lastel on pankurooniumi vajadus veidi suurem.
Pankuroonium vabaneb lahuse kujul, millest 1 ml sisaldab 1-2 mg ravimit. Pankurooniumi tuleb hoida külmkapis temperatuuril 2–8 ° C.
Kõrvaltoimed ja rakenduse omadused
A. Arteriaalne hüpertensioon ja tahhükardia. Pankurooniumi mõju vereringele on tingitud vaguse närvi blokaadist ja katehhoolamiinide vabanemisest adrenergiliste närvide otstest. Pankurooniumi tuleb kasutada ettevaatusega juhtudel, kui tahhükardia teke on suurenenud riskitegur (koronaararterite haigus, hüpertroofiline kardiomüopaatia).
B. Arütmiad. Suurenenud atrioventrikulaarne juhtivus ja katehhoolamiinide vabanemine suurendavad riskirühma kuuluvatel patsientidel ventrikulaarsete arütmiate tõenäosust. Arütmiarisk on eriti suur, kui seda kombineerida pankurooniumi, tritsükliliste antidepressantide ja halotaaniga.
B. Allergilised reaktsioonid. Ülitundlikkuse korral bromiidide suhtes võib tekkida allergia pankurooniumi (pankurooniumbromiidi) suhtes.
Vecuronium
Struktuur
Vecuronium on pankuroonium, millel puudub metüülkvaternaarne rühm (st see on monokvaternaarne ammooniumiühend). Kerge struktuurne erinevus vähendab kõrvaltoimete raskust ilma võimsust mõjutamata.
Ainevahetus ja eritumine
Vähesel määral toimub vekurooniumi metabolism maksas. Vecuroon eritub peamiselt sapiga, vähemal määral neerude kaudu (25%). Neerupuudulikkuse korral on soovitatav kasutada vekurooniumi, kuigi mõnikord pikendab see seisund ravimi toimet. Vekurooniumi lühike toimeaeg on seletatav lühema poolväärtusajaga eliminatsioonifaasis ja kiirema kliirensiga võrreldes pankurooniumiga. Pikaajaline vekurooniumi kasutamine intensiivravi osakonnas põhjustab patsientidel pikaajalist neuromuskulaarset blokaadi (kuni mitu päeva), mis võib olla tingitud 3-hüdroksümetaboliidi kuhjumisest või polüneuropaatia tekkest. Riskifaktoriteks on naissoost olemine, neerupuudulikkus, kortikosteroidide pikaajaline kasutamine ja sepsis. AIDSi korral on vekurooniumi toime pikenenud. Pikaajalisel kasutamisel areneb ravimi taluvus.
Annustamine
Vecuronium on sama efektiivne kui pankuroonium. Intubatsiooniks vajalik annus on 0,08-0,12 mg / kg. Intraoperatiivse lihaslõõgastuse laadimisannus on 0,04 mg / kg, säilitusannus on 0,01 mg / kg iga 15-20 minuti järel. Infusioon annuses 1-2 μg / (kg x min) võimaldab teil saavutada ka hea lõõgastuse.
Vanus ei mõjuta küllastusannuse vajadust, samas kui vastsündinutel ja imikutel peaksid säilitusannuste vahelised intervallid olema pikemad. Äsja sünnitanud naistel pikeneb vekurooniumi toime kestus maksa verevoolu muutuste ja ravimi maksa kaudu imendumise tõttu.
Vecuronium on pakendatud 10 mg pulbri kujul, mis lahustatakse vahetult enne manustamist säilitusainevabas vees. Lahjendatud ravimit võib kasutada 24 tunni jooksul.
Kõrvaltoimed ja rakenduse omadused
A. Vereringe. Isegi annuses 0,28 mg / kg ei mõjuta vekuroonium vereringet.
B. Maksapuudulikkus. Kuigi vekurooniumi eliminatsiooni määrab eritumine sapiga, pikendab maksapuudulikkuse esinemine veidi ravimi toime kestust - eeldusel, et annus ei ületa 0,15 mg / kg. Maksasiirdamise anhepaatilises faasis vekurooniumi vajadus väheneb.
Pipekuroonium
Struktuur
Pipekuroonium on steroidstruktuuriga bis-kvaternaarne ammooniumiühend, mis on väga sarnane pankurooniumiga.
Ainevahetus ja eritumine
Nagu ka teiste pikatoimeliste mittedepolariseerivate lihasrelaksantide puhul, on metabolismil pipkurooniumi eliminatsioonil väike roll. Eliminatsioon määratakse eritumisega, mis toimub peamiselt neerude (70%) ja sapi (20%) kaudu. Toime kestus pikeneb neeru-, kuid mitte maksapuudulikkusega patsientidel.
Annustamine
Pipekuroonium on veidi tugevam kui pankuroonium. Intubatsiooniks vajalik annus on 0,06-0,1 mg / kg. Lihaslõõgastuse intraoperatiivseks säilitamiseks kasutatavad annused on 20% väiksemad kui pankurooniumi puhul. Imikutel on ravimi vajadus kehakaalu kilogrammi kohta suurem kui vanematel lastel ja täiskasvanutel. Vanadus praktiliselt ei mõjuta pipkurooniumi farmakoloogilist profiili.
Kõrvaltoimed ja rakenduse omadused
Pipkurooniumi peamine eelis pankurooniumi ees on kõrvaltoimete puudumine vereringele. Pipekuroonium ei käivita histamiini vabanemist. Nende ravimite toime algus ja kestus on sarnased.
Rokuroonium
Struktuur
See vekurooniumi monokvaternaarne steroidanaloog on sünteesitud, et tagada kiire toime algus.
Ainevahetus ja eritumine
Rokuroonium ei metaboliseeru ja eritub peamiselt sapiga ja vähemal määral neerude kaudu. Toime kestus pikeneb maksapuudulikkusega patsientidel, samas kui neerupuudulikkuse esinemine ei avalda erilist mõju ravimi farmakokineetikale.
Annustamine
Rokurooniumi võimsus on väiksem kui teistel steroidsete lihasrelaksantide omal (jõud on pöördvõrdeline toime avaldumise kiirusega). Intubatsiooniks vajalik annus on 0,45-0,6 mg / kg. Intraoperatiivse lihaslõõgastuse säilitamiseks manustatakse ravimit boolusena annuses 0,15 mg / kg. Infusiooniannus on vahemikus 5 kuni 12 μg / (kg x min). Rokurooniumi toimeaeg eakatel patsientidel pikeneb oluliselt.
Kõrvaltoimed ja rakenduse omadused
Rokuroonium (0,9–1,2 mg/kg) on ainus mittedepolariseeriv lihasrelaksant, mis toimib sama kiiresti kui suktsinüülkoliin, mistõttu on see valitud ravim kiireks järjestikuseks induktsiooniks. Rokurooniumi keskmine toimeaeg on sarnane vekurooniumi ja atrakuuriumi omaga. Rokuroonium annab veidi tugevama vagolüütilise toime kui pankuroonium.
Juhtumiuuring: hiline ärkamine pärast üldanesteesiat
72-aastasele mehele tehti transuretraalne resektsioon eesnäärmeüldnarkoosis. 20 minuti jooksul pärast operatsiooni lõppu ei ole patsient veel spontaanset hingamist ja teadvust taastunud.
Milline on selles olukorras tavaline diagnostiline lähenemisviis?
Vajalik on uurida anamneesi, sealhulgas kasutatud ravimeid, läbi viia füüsikalisi ja laboratoorseid uuringuid ning analüüsida tehtud anesteesiat.
Millised haigused suurendavad teadvuse taastumise ja neuromuskulaarse juhtivuse hilinemise ohtu?
Arteriaalse hüpertensiooni korral on aju verevoolu autoregulatsioon häiritud, mis vähendab aju taluvust hüpotensiooni episoodide suhtes. Maksahaiguse korral väheneb maksa metabolism ravimid ja nende eritumine sapiga, mis pikendab kestust
Nende ravimite toime. Albumiini kontsentratsiooni vähenemine vereseerumis suurendab ravimi vaba (ja vastavalt ka aktiivset) fraktsiooni. Maksa entsefalopaatia põhjustab teadvuse häireid. Neeruhaiguste korral on paljude ravimite eritumine häiritud. Ureemia mõjutab ka teadvuse taset. Suhkurtõbi on seotud hüpoglükeemia ja hüperosmolaarse hüperglükeemilise mittetsütoatsidootse kooma riskiga. Müra unearterite kohal koos ajuisheemia sümptomitega ja anamneesis insult suurendab intraoperatiivsete tserebrovaskulaarsete õnnetuste riski. Intrakardiaalne bypass operatsioon, eriti kaasasündinud südamerikkega lastel, võib põhjustada paradoksaalset õhuembooliat: defektide kaudu tulevad õhumullid venoossest süsteemist arteriaalsesse süsteemi, sealhulgas ajuarteritesse. Paradoksaalne õhuemboolia võib põhjustada püsivat ajukahjustust. Raske hüpotüreoidism muudab ravimite metabolismi ja harvadel juhtudel põhjustab mükseemi kooma.
Kui kitsas on diagnostiline otsing eelneva tüsistusteta üldanesteesia ajalooga?
Tüsistusteta eelnev üldanesteesia, mille käigus kasutati suktsinüülkoliini, võimaldab välistada pseudokoliinesteraasi kaasasündinud defekti. Normaalse pseudokoliinesteraasi kontsentratsiooni langus ei põhjusta operatsioonijärgset apnoed, välja arvatud äärmiselt lühiajalised sekkumised. Pahaloomuline hüpertermia ei avaldu tavaliselt hilinenud ärkamisena, kuigi see pikendab anesteetikumide hüpnootilist toimet. Tüsistusteta eelnev üldanesteesia ei välista pahaloomulist hüpertermiat. Anamneesis anesteesiast hiline ärkamine võib viidata ülitundlikkusele anesteetikumide suhtes (nt eakatel).
Kas haigete inimeste kodus võetavad ravimid võivad mõjutada ärkamist?
MAC-i alandavad ravimid (nt reserpiin või metüüldopa) suurendavad anesteetikumi üleannustamise riski. Äge alkoholimürgitus pärsib barbituraatide ainevahetust ja annab sellest hoolimata rahustava toime. Maksafunktsiooni vähendavad ravimid
Verevool (nt tsimetidiin) aeglustab maksa metabolismi. Parkinsonismi raviks kasutatavad ravimid ja tritsüklilised antidepressandid, millel on tsentraalne antikolinergiline toime, võimendavad skopolamiini põhjustatud sedatsiooni. Pikatoimelised rahustid, nagu bensodiasepiinid, aeglustavad ärkamist.
Kas anesteesia tehnika mõjutab ärkamise kiirust?
Premedikatsioonitehnikal võib olla mõju ärkamisele. Eriti aeglustab teadvuse taastumist operatsioonijärgsel perioodil, antikolinergiliste ainete (välja arvatud glükopürrolaat, mis ei tungi läbi hematoentsefaalbarjääri), opioidide ja rahustite kasutamine. Madal südame väljund aeglustab intramuskulaarsel manustamisel ravimi imendumist.
Anesteesia säilitamise meetod mõjutab ka ärkamise kiirust. Dilämmastikoksiidi kombinatsiooni opioididega (näiteks fentanüüliga) seostatakse varajaste ärkamissümptomite kiire ilmnemisega, nagu silmade avamine või suuliste juhiste järgimine. Täieliku ärkamise määr on aga ligikaudu sama nii inhalatsioonianesteesia kui ka dilämmastikoksiidi ja opioidide kombinatsiooni puhul.
Operatsioonijärgse uneapnoe levinud põhjus on hüperventilatsioon operatsiooni ajal. Kuna inhalatsioonianesteetikumid tõstavad apnoe läve (nii nimetatakse maksimaalset PaCO2 väärtust, mille juures patsient ei hakka iseseisvalt hingama), on hingamiskeskuse stimuleerimiseks soovitatav mõõdukas operatsioonijärgne hüpoventilatsioon. Raske operatsioonisisene hüpo- või hüpertensioon suurendab hüpoksia ja ajuturse riski.
Hüpotermia alandab MAC-i, pärsib neuromuskulaarse juhtivuse taastumist ja pärsib ravimite metabolismi. Arteriaalne hüpoksia ja raske hüperkapnia (PaCO2> 70 mm Hg) põhjustavad teadvuse häireid.
Mõned kirurgilised sekkumised (nt unearteri endarterektoomia, südame-kopsuoperatsioon, ajuoperatsioon) on seotud operatsioonijärgse neuroloogilise defitsiidi suurenenud riskiga. Lahjendushüponatreemia on tavaline pärast eesnäärme transuretraalset resektsiooni niisutuslahuse imendumise tõttu.
Milliseid sümptomeid füüsiline läbivaatus paljastab?
Pupilli läbimõõt ei ole alati piisav näitaja. Sellegipoolest, kui antikolinergiliste ainete ja ganglionide blokaatorite (trimetafaan) kasutamine on välistatud, on laiad fikseeritud pupillid ähvardav sümptom. Reaktsioon valulikule stiimulile (nt sunnitud edasiliikumine alalõug) võimaldab piiritleda teadvuse rõhumise lihaste lõdvestusest. Perifeersete närvide stimulatsioonil on sama eesmärk.
Milliseid laboratoorseid ja instrumentaalseid uurimismeetodeid saab soovitada?
Soovitatav on uurida arteriaalse vere gaase ja seerumi elektrolüüte, eriti naatriumi. Konsultant neuroloog võib tellida aju CT-skanni.
Millist ravi tuleks määrata?
On vaja jätkata mehaanilist ventilatsiooni. Sõltuvalt hilinenud ärkamise põhjusest võib kasutada naloksooni, flumaseniili, füsostigmiini, doksapraami või aminofülliini.
Skeletilihaste lõdvestamist võivad põhjustada regionaalne anesteesia, inhalatsioonianesteetikumide suured annused ja neuromuskulaarset ülekannet blokeerivad ravimid (nende üldnimetus on lihasrelaksandid). 1942. aastal avaldas Harold Griffith kurare (mürk, mida Lõuna-Ameerika indiaanlased kasutasid nooleotste määrimiseks) puhastatud ekstrakti anesteesias kasutamise kohta. Lihasrelaksandid said kiiresti anestesioloogi ravimiarsenali lahutamatuks osaks. Nagu Griffith märkis, põhjustavad lihasrelaksandid pigem skeletilihaste lõdvestamist kui anesteesiat.
N.B. Lihasrelaksandid ei põhjusta teadvusekaotust, amneesiat ega analgeesiat.
Neuromuskulaarne ülekanne
Kohta, kus motoorne neuron puutub kokku lihasrakuga, nimetatakse neuromuskulaarne sünaps(vt joonist). Motoorse neuroni ja lihasrakkude rakumembraane eraldab kitsas vahe (20 nm) - sünaptiline lõhe. Kui aktsioonipotentsiaal depolariseerib motoorsete neuronite terminali, sisenevad kaltsiumiioonid väljastpoolt närvi tsütoplasmasse, mis põhjustab sulandumise presünaptilise terminaalse membraaniga sünaptilised vesiikulid ja neis sisalduva atsetüülkoliini vabanemine sünaptilisse pilusse.
Joonistamine.
Atsetüülkoliini molekulid difundeeruvad läbi sünaptilise pilu ja interakteeruvad nikotiinitundlikud kolinergilised retseptorid(n-kolinergilised retseptorid) lihasraku membraani spetsiifilises osas - skeletilihase otsaplaat.
Iga kolinergiline retseptor koosneb viiest valgu subühikust, millest kaks (α-subühikud) on samad ja on võimelised siduma atsetüülkoliini molekule (üks α-subühik – üks sidumissait). Kui mõlemad seondumiskohad on hõivatud kahe atsetüülkoliini molekuliga, siis muutub alaühikute konformatsioon, mis toob kaasa lühiajalise (1 ms) retseptori paksust läbiva ioonikanali avanemise (vt joonist).
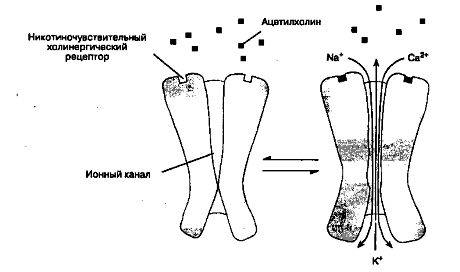
Joonistamine... Atsetüülkoliini seondumine skeletilihase otsaplaadi retseptoriga avab kanali ja indutseerib ioonivoolu
Läbi avatud kanali hakkavad voolama katioonid (naatrium ja kaltsium - väljastpoolt raku sisemusse, kaalium - rakust väljapoole), mis põhjustab välimuse. otsaplaadi potentsiaal. Ühe sünaptilise vesiikuli – kvanti atsetüülkoliini – sisaldus põhjustab miniatuurse otsaplaadi potentsiaal(1 kvant - 10 000 atsetüülkoliini molekuli). Kui atsetüülkoliini poolt on hõivatud piisav arv retseptoreid, muutub otsaplaadi kogupotentsiaal piisavalt võimsaks, et depolariseerida sünapsi ümbritsev postsünaptiline membraan. Naatriumikanalid lihasraku membraani selles osas avanevad potentsiaalide erinevuse mõjul (erinevalt otsaplaadi retseptorite kanalitest, mis avanevad koostoimel atsetüülkoliiniga). Tekkiv tegevuspotentsiaal levib mööda lihasraku membraani ja T-tuubulite süsteemi, mis põhjustab naatriumikanalite avanemise ja kaltsiumiioonide vabanemise sarkoplasmaatilise retikulumi tsisternidest. Vabanenud kaltsium vahendab kontraktiilsete valkude aktiini ja müosiini koostoimet, mis viib lihaskiudude kokkutõmbumiseni. Vabanenud atsetüülkoliini kogus ületab tavaliselt aktsioonipotentsiaali arendamiseks vajaliku miinimumi. Mõned haigused häirivad neuromuskulaarse ülekande protsessi: müasteenilise Eaton-Lamberti sündroomi korral vabaneb ebapiisav kogus atsetüülkoliini, myasthenia gravis'e korral (müasteeniagravis) kolinergiliste retseptorite arv väheneb.
Substraadi spetsiifiline ensüüm atsetüülkoliinesteraas hüdrolüüsib atsetüülkoliini kiiresti äädikhappeks ja koliiniks. Selle ensüümi molekulid (nimetatakse ka konkreetne, või tõsi, koliinesteraas) on fikseeritud otsaplaadis kolinergiliste retseptorite vahetusse lähedusse. Lõppkokkuvõttes suletakse ioonikanalid, mille tulemuseks on otsaplaadi repolarisatsioon. Kui aktsioonipotentsiaali levik peatub, sulguvad ka lihaskiu membraanis olevad ioonikanalid. Kaltsium siseneb tagasi sarkoplasmaatilisesse retikulumi ja lihaskiud lõdvestuvad.
Depolariseeriv ja mittedepolariseeriv plokk
Lihasrelaksandid jagunevad kahte klassi: depolariseerivad ja mittedepolariseerivad (vt tabelit). See alajaotus peegeldab erinevusi toimemehhanismis, reaktsioonis perifeerse närvi stimulatsioonile ja sellele järgnevas neuromuskulaarse juhtivuse taastamises.
| Depolariseerivad lihasrelaksandid |
Mittedepolariseerivad lihasrelaksandid |
| Lühike näitlemine | Pikatoimeline |
| Suktsinüülkoliin | Tubokurariin |
| Dekametoonium | Metokurin |
| Doksakuurium | |
| Pankuroonium | |
| Pipekuroonium | |
| Gallamiin | |
| Keskmine kestus | |
| Atrakuurium | |
| Vecuronium | |
| Rokuroonium | |
| Lühike näitlemine | |
| Mivakuurium |
TABEL... Depolariseerivad ja mittedepolariseerivad lihasrelaksandid
Toimemehhanism
depolariseerivad lihasrelaksandid, meenutavad struktuurilt atsetüülkoliini, interakteeruvad n-kolinergiliste retseptoritega ja põhjustavad lihasraku aktsioonipotentsiaali. Kuid erinevalt atsetüülkoliinist depolariseerivad lihasrelaksandid ei ole hüdrolüüsitud atsetüülkoliinesteraas ja nende kontsentratsioon sünaptilises pilus ei vähene pikka aega, mis põhjustab terminaalplaadi pikaajalist depolarisatsiooni.
Terminaalplaadi pikaajaline depolarisatsioon viib lihaste lõdvestumiseni. Lihaste lõdvestumine toimub järgmiselt: nagu varem mainitud, on otsaplaadi võimas potentsiaal võimeline depolariseerima sünapsi ümbritsevat postsünaptilist membraani. Hilisem naatriumikanalite avanemine on aga lühiajaline. Pärast esialgset ergastamist ja avamist kanalid suletakse. Lisaks ei saa naatriumikanalid uuesti avaneda enne, kui otsaplaat on repolariseerunud. Terminalplaadi repolarisatsioon on omakorda võimatu seni, kuni depolariseeriv lihasrelaksant on seotud kolinergiliste retseptoritega. Kuna sünapsi ümbritsevas membraanis on kanalid suletud, siis aktsioonipotentsiaal kuivab ja lihasraku membraan repolariseerub, mis põhjustab lihaste lõdvestamist. Seda neuromuskulaarse juhtivuse blokaadi nimetatakse tavaliselt madepolariseeriva ploki faas.
Mittedepolariseerivad lihasrelaksandid seonduvad ka kolinergiliste retseptoritega, kuid see ei too kaasa konformatsioonilisi muutusi, mis põhjustavad kanali avanemist. Kuna sel juhul atsetüülkoliin retseptoritega ei interakteeru, siis otsaplaadi potentsiaali ei teki.
N.B. Depolariseerivad lihasrelaksandid toimivad kolinergiliste retseptorite agonistidena, mittedepolariseerivad aga konkureerivate antagonistidena.
See toimemehhanismi peamine erinevus seletab ravimite toime erinevust organismile mõne haiguse korral. Näiteks atsetüülkoliini vabanemise krooniline vähenemine (traumaatilise lihaste denervatsiooni korral) stimuleerib kolinergiliste retseptorite kompenseerivat suurenemist skeletilihaste otsplaatides. See võimendab depolariseerivate lihasrelaksantide toimet (ülesregulatsioon – rohkem retseptoreid on depolariseerunud), kuid nõrgestab mittedepolariseerivate lihasrelaksantide toimet (blokeerida tuleb rohkem retseptoreid). Kolinergiliste retseptorite arvu vähenemine (näiteks myasthenia gravis'e allareguleerimine), vastupidi, nõrgestab depolariseerivate lihasrelaksantide toimet ja võimendab mittedepolariseerivate ainete toimet.
Vastus perifeerse närvi stimulatsioonile
Siin on käsitletud neuromuskulaarse ülekande jälgimist perifeerse närvi stimuleerimise ja esilekutsutud lihasreaktsiooni salvestamise kaudu. Stimuleerimiseks kasutatakse ruudukujulisi elektrilisi supramaksimaalseid impulsse. Laialdaselt kasutatakse nelja stimuleerimisviisi.
Tetaniline stimulatsioon: pidev impulsside jada sagedusega 50-100 Hz, rakendatakse 5 s.
Üks stiimul:üksikimpulss kestusega 0,2 msek.
Nelja impulsi seeria (ingliskeelne nimi -rong kohta neli, lühendatultTOF; tulevikus üldtunnustatud mõiste "TOF-režiim"): neljast impulssist koosnev jada, igaüks kestusega 0,2 ms ja mida rakendatakse 2 s (sagedus 2 Hz).
Kahekordne välklambi stimulatsioon(SRDV): kolmest lühikesest (0,2 msek) impulssist koosnev jada intervalliga 20 ms (sagedus 50 Hz), seejärel 750 ms pikkune paus, mille järel korratakse kahte (SRDV3.2) või kolme (SRDV3.3) impulssi sarnaselt esialgsed.
sumbumine, see tähendab, et esilekutsutud lihasreaktsiooni järkjärguline vähenemine koos närvi pikaajalise või korduva stimulatsiooniga on iseloomulik mittedepolariseerivate lihasrelaksantide toimele. Sumbumist seletatakse asjaoluga, et mittedepolariseerivad lihasrelaksandid vähendavad närvistimulatsiooni käigus vabaneva atsetüülkoliini hulka (atsetüülkoliini mobilisatsiooni blokaad). Neuromuskulaarse juhtivuse täielik taastamine on selgelt korrelatsioonis nõrgenemise puudumisega. Kuna teetanilise stimulatsiooni ja topeltvälgu režiimis stimuleerimise korral on nõrgenemine paremini tuvastatav kui TOF-režiimis ja korduvate üksikute stiimulite korral, on neuromuskulaarse juhtivuse taastamise kasulikkuse hindamiseks eelistatav kasutada kahte esimest režiimi. anesteesiast.
Tetaanilise stimulatsiooni võimet suurendada vastust ühele impulsile nimetatakse post-teetaniline leevendus... Teetaanijärgne leevendus võib olla tingitud atsetüülkoliini mobilisatsiooni kompenseerivast suurenemisest pärast teetanilist stimulatsiooni.
Erinevalt mittedepolariseerivast plokist
- Depolariseeriva ploki I faasi ei iseloomusta sumbumine teetanilise stimulatsiooni ajal ja TOF-režiimis ning puudub post-teetaniline leevendus. Kui aga depolariseeriva lihasrelaksandi annus on liiga suur, muutub ploki kvaliteet – see hakkab meenutama mittedepolariseerivat.
- Depolariseeriva ploki II faas ja seda saab seletada ioonsete ja konformatsiooniliste muutustega, mis tekivad lihasraku pikaajalisel depolarisatsioonil.
Neuromuskulaarse juhtivuse taastamine
N.B. Depolariseerivad lihasrelaksandid ei interakteeru atsetüülkoliinesteraasiga. Neuromuskulaarse sünapsi piirkonnast sisenevad nad vereringesse, mille järel nad hüdrolüüsivad plasmas ja maksas teise ensüümi - pseudokoliinesteraasi (sünonüümid - mittespetsiifiline koliinesteraas, plasma koliinesteraas) toimel.
See protsess kulgeb väga kiiresti, millel on soodne iseloom: depolariseeriva ploki jaoks pole spetsiifilisi antidoote.
Mittedepolariseerivaid lihasrelaksante, välja arvatud mivakuurium, ei hüdrolüüsi ei atsetüülkoliinesteraas ega pseudokoliinesteraas. Mittedepolariseeriva blokaadi korral on neuromuskulaarse juhtivuse taastamine tingitud mittedepolariseerivate lihasrelaksantide ümberjaotumisest, osalisest metaboolsest lagunemisest ja eritumisest või võib selle põhjustada spetsiifiliste antidootide - atsetüülkoliinesteraasi inhibiitorite - toime. Kuna atsetüülkoliinesteraasi inhibiitorid suurendavad saadaoleva atsetüülkoliini kogust, mis konkureerib depolariseerivate lõõgastajatega neuromuskulaarsetes sünapsides, ei suuda nad depolariseerivat plokki kõrvaldada. Tegelikult suurendavad atsetüülkoliinesteraasi inhibiitorid saadaoleva atsetüülkoliini kontsentratsiooni neuromuskulaarses sünapsis ja vähendavad plasma pseudokoliinesteraasi aktiivsust, suurendades depolariseeriva blokaadi kestust.
Lihasrelaksandid lõdvestavad skeletilihaseid, mis hõlbustab kirurgilist juurdepääsu ja hingetoru intubatsiooni ning võimaldab piirata teiste anesteetikumide väikeseid annuseid.
Üks olulisi riske lihasrelaksantide kasutamisel ilma piisava koguse narkootilise või sissehingatava ravimita on tõenäosus, et halvatud patsient jääb aja jooksul ärkvel ja ärkvel. Viimane on äärmiselt haruldane, kuid viib vastavate psühholoogiliste ja kohtuekspertiisi tagajärgedeni. Toimemehhanismi alusel jagatakse lihasrelaksandid depolariseerivateks ja mittedepolariseerivateks aineteks.
Depolariseerivad lihasrelaksandid
Kliiniliseks kasutamiseks on praegu saadaval ainult üks depolariseeriv lihasrelaksant – suktsinüülkoliin (suksametoonium, ditiliini). Seda iseloomustab kiire algus (15–30 s) ja lühike toimeaeg (3–5 minutit). Patsientidel, kellel on operatsiooni ajal kõht täis, kasutatakse suktsinüülkoliini sageli kiireks järjestikuseks induktsiooniks (intraoperatiivne ravi).
Lihasrelaksant suktsinüülkoliin põhjustab postsünaptilise membraani depolarisatsiooni mehhanismi abil, mis meenutab atsetüülkoliini toimet. Ravim kutsub esmalt esile ajutised lihaskontraktsioonid, mida nimetatakse fascikulatsioonideks, millele järgneb lõõgastusfaas. Seda lihasrelaksanti metaboliseerib plasma koliinesteraas ja sellel puudub spetsiifiline antagonist.
Suktsinüülkoliini kõrvaltoimete hulka kuuluvad bradükardia (eriti lastel), hüperkaleemia, silmasisese ja intrakraniaalse rõhu tõus, pahaloomuline hüpertermia (tundlikel isikutel) ja operatsioonijärgsed müalgiad. kaela, õlgade ja kõhuseina lihastes põhjustavad tugevat nõrkust, eriti kontekstis.
Mittedepolariseerivad lihasrelaksandid
Mittedepolariseerivad lõõgastajad seonduvad neuromuskulaarsete retseptoritega, mille pärast nad konkureerivad atsetüülkoliiniga, mis põhjustab aktivatsiooni. Skeletilihaste lõdvestamiseks peab ravim hõivama rohkem kui 70% retseptoritest. Toimingu alguseni võib kuluda mõni minut. Nende ravimite toime kõrvaldatakse sobivate vahenditega.
Mõju kestuse alusel jagatakse lihasrelaksandid lühikese, keskmise ja pika toimeajaga ravimiteks. Erilist tähelepanu tuleb pöörata kõrvaltoimetele südame-veresoonkonna süsteem ja ainevahetuse erinevused võimaldavad igal patsiendil valida endale sobivaima vahendi.
Lühitoimelised lihasrelaksandid. Mivakuurium hakkab kiiresti toimima, metaboliseerub plasma koliinesteraasi poolt ja farmakoloogilisi antagoniste pole vaja.
Keskmise kestusega lihasrelaksandid. Nende hulka kuuluvad atrakuuria besülaat, tsisatrakuuria besülaat, vekurooniumbromiid, rokurooniumbromiid. Atrakuuriat, sõltumata annusest, iseloomustab spontaanne in vivo lagunemine (Hoffmani eliminatsioon), suurte annuste kasutamisega kaasneb histamiini vabanemine. Tsisatrakuuriumbesülaat on omadustelt sarnane atrakuuriumbesülaadiga, kuid seda iseloomustab aeglasem toime algus ja minimaalne histamiini vabanemine. Vecurooniumbromiid eritub neerude kaudu ja sellel on väga väike mõju südame-veresoonkonna süsteemile. Rokurooniumbromiid hakkab kiiresti toimima ja mõjutab minimaalselt ka hemodünaamikat. Tahhükardia ja raske bradükardia ennetamine on koronaararterite haigusega patsientidel ülioluline.
^ KÕRVALMÕJUD1. Allergilised reaktsioonid kuni anafülaktiliseks. 2. Kõige tavalisem lihasvalu pärast suktsinüülkoliini kasutamist. Ennetamine seisneb läbiviimises eelkuraatoriks seadmine, st. mittedepolariseeriva lihasrelaksandi kasutuselevõtt mõni minut enne suktsinüülkoliini süstimist, kuigi see meede ei ole alati efektiivne. Alternatiiviks prekursoriseerimisele on intravenoosne manustamine ka mõni minut enne suktsinüülkoliini lidokaiini. 3. Südame rütmihäired ja arteriaalne hüpotensioon Seotud histamiini vabanemisega ja ganglionide blokaadiga. Võib põhjustada tõsist bradükardiat ja isegi südameseiskust hüperkaleemia vastuseks depolariseerivate lihasrelaksantide kasutuselevõtule raskete traumade, põletuste korral. 4. Lihasrelaksantide pikaajaline jääkmõju hüpovoleemia, vereringehäirete, elektrolüütide tasakaaluhäirete ja atsidoosi korral võib see põhjustada pikaajalist apnoed. 5. Maosisu regurgitatsioon ja aspiratsioon trahheobronhiaalpuusse "täis" kõhuga patsientidel. Profülaktika eesmärgil on soovitatav kõhtu tühjendada sondiga, tagada pea ja torso kõrgendatud asend. Lisaks on premedikatsioonis soovitatav kasutada mao sekretsiooni vähendavaid ravimeid (näiteks H 2 -histamiini retseptorite blokaatorid). 6. Pahaloomuline hüpertermia on suktsinüülkoliini kasutamisel kõige ohtlikum tüsistus. Pahaloomuline hüpertermia- kaltsiumi metabolismi funktsionaalsed häired lihasfüsioloogia patoloogiliste kõrvalekallete korral, kuigi kahjustatud on ka muud kaltsiumiga seotud struktuurid (müokard, närvid, trombotsüüdid, lümfotsüüdid jne). Sündroom võib areneda nii anesteesia esilekutsumisel kui ka mitu tundi pärast selle lõppu. Levinumad käivitajad- suktsinüülkoliin ja halotaan, kuigi need võivad olla ka muud ravimid (kalipsool, lidokaiin jne). Pahaloomulist hüpertermiat võivad süvendada adrenaliin, südameglükosiidid, kaltsiumisoolad, teofülliini derivaadid. Pipekuroonium (arduaan) Ravim ei põhjusta histamiini vabanemist ega mõjuta vereringet.0,07 mg / kg manustamisel tekivad optimaalsed tingimused intubatsiooniks 3 minuti pärast ja kliiniliselt efektiivne blokaad kestab 70 minutit. Pankuroonium (pavulon) Ravimi eripäraks on selle võime blokeerida vaguse mõju ja vabastada katehhoolamiine adrenergilistest närvilõpmetest, samuti pärssida norepinefriini taasjoomist. Mis puudutab kõrvalmõjud ravim on tahhükardia, mõõdukas hüpertensioon, arütmia, suurenenud müokardi hapnikuvajadus Praktikas kasutatakse kõige sagedamini: ditiliin, arduaan, diplatsiin
Lihasrelaksandid on ravimid, mis lõdvestavad vöötlihaseid.
Sellest artiklist saate teada lihasrelaksantide klassifikatsiooni ja lihasrelaksantide toimimise anestesioloogias.
Lihasrelaksantide toime
Kuidas lihasrelaksante kasutatakse?
Neid kasutatakse peamiselt endotrahheaalseks intubatsiooniks. Lihasrelaksantide väga oluline toime on kõigi vabatahtlike lihaste refleksitegevuse vältimine. Anesteesia ajal ilma lihasrelaksante kasutamata säilitavad lihased piisava toonuse, mis võib takistada kirurgi tegevust. Lisaks võimaldab lihasrelaksantide kasutamine anestesioloogil manustada anesteesiat, kasutades anesteetikumide väiksemaid annuseid, mis loomulikult vähendab anesteesia ohtu.
On väga oluline, et need ravimid, mis põhjustavad täielikku neuromuskulaarset blokaadi, vähendaksid järsult lihastest kesknärvisüsteemi suunduvaid patoloogilisi impulsse. Järelikult aitab lihaste lõdvestamine koos teiste üldanesteesia komponentidega saavutada patsiendi tõhusa kaitse operatsioonistressi eest.
Lisaks kasutatakse lihasrelaksante lihasspasmide ennetamiseks selliste haiguste puhul nagu teetanus, marutaudi, epileptiline seisund ja mis tahes etioloogiaga mitterefraktaarsed krambid.
Lihasrelaksantide klassifikatsioon
On hästi teada, et kõik lihasrelaksandid jagunevad sõltuvalt nende toimemehhanismist kahte suurde rühma: depolariseerivad ja mittedepolariseerivad (konkureerivad). Nende toimemehhanismi ettekujutamiseks on vaja lühidalt käsitleda neuromuskulaarse ülekande füsioloogiat.
Neuromuskulaarse ülekande füsioloogia
Motoorse närvi iga haru lõpeb neuromuskulaarse sünapsiga. See koosneb kahest membraanist: närvilõpmete membraanist (presünaptiline) ja lihaskiudude membraanist (postsünaptiline või motoorne otsaplaat). Membraanide vahel on umbes 500 angströmi pikkune sünaptiline vahe, mis on täidetud geeli konsistentsiga vedelikuga. Impulsside ülekandmine närvist lihaskiule toimub atsetüülkoliini vabanemisega, mis sünteesitakse ja säilitatakse presünaptilises terminalis.
Puhkeolekus on mootori otsaplaat polariseeritud olekus, sisemembraanil on negatiivne elektrilaeng ja membraani välispinnal positiivne elektrilaeng.
Motoorse närvi ärrituse korral vabaneb atsetüülkoliin, mis läbib presünaptilist membraani ja valgub sünaptilisse pilusse. Seal interakteerub see mootori otsaplaadi kolinergiliste retseptoritega.
Kui atsetüülkoliin ühineb retseptoritega, täheldatakse postsünaptilise membraani läbilaskvuse järsku muutust, peamiselt naatriumi- ja kaaliumiioonide puhul. Selle tulemuseks on motoorse otsaplaadi depolarisatsioon ja lokaalse potentsiaali tekkimine sellel, millele järgneb lihaskiu kokkutõmbumine.
Atsetüülkoliin lakkab millisekundite jooksul pärast kolinergiliste retseptoritega seondumist toimimast koliinesteraasi mõjul, mis lagundab selle koliiniks ja äädikhappeks. Selle tulemusena postsünaptiline membraan repolariseerub ja lihaskiud lõdvestuvad.
Depolariseerivad ja mittedepolariseerivad lihasrelaksandid
Mittedepolariseerivate lihasrelaksantide toimemehhanism seisneb selles, et neil on afiinsus atsetüülkoliini retseptorite suhtes ja nad konkureerivad atsetüülkoliiniga võime pärast nendega seonduda, takistades vahendaja juurdepääsu retseptoritele. Konkureerivate neuromuskulaarsete blokaatoritega kokkupuute tagajärjel on postsünaptiline membraan püsiva polarisatsiooni seisundis ja kaotab oma depolariseerumisvõime. Seetõttu kaotab lihaskiud oma kokkutõmbumisvõime.
Mittedepolariseerivate lihasrelaksantide põhjustatud neuromuskulaarse blokaadi saab lõpetada antikoliinesteraasi ravimite (proseriin, neostigmiin, galantamiin) manustamisega. Nad on võimelised blokeerima koliinesteraasi ja seega takistama atsetüülkoliini lagunemist. Sel juhul nihkub konkurents postsünaptilise membraani retseptorite pärast loomuliku vahendaja poole ja taastub neuromuskulaarne juhtivus.
Depolariseerivate lihasrelaksantide müoparalüüsiv toime on seotud asjaoluga, et need toimivad postsünaptilisele membraanile nagu atsetüülkoliin, depolariseerides seda ja põhjustades lihaskiudude stimulatsiooni. Kuid kuna neid ei eemaldata koheselt retseptorist ja nad blokeerivad juurdepääsu atsetüülkoliinile, on depolarisatsioon suhteliselt pikk ja ebapiisav, et hoida lihaseid kokkutõmbunud olekus. Seetõttu viimane lõdvestab.
Loomulikult on antikoliinesteraasi ravimite kasutamine depolariseerivate lihasrelaksantide antidootidena ebaefektiivne, kuna akumuleerunud atsetüülkoliin suurendab ainult terminaalse membraani depolarisatsiooni ja seetõttu suurendab, mitte ei vähenda neuromuskulaarse blokaadi astet.
Lõõgastite toime teine faas
Huvitav on see, et kõigil juhtudel isegi ühekordse depolariseerivate lihasrelaksantide manustamise korral, rääkimata korduvate annuste kasutuselevõtust, leitakse postsünaptilisel membraanil ühe või teise astme muutusi, mis seisnevad selles, et depolariseeriva blokaadiga kaasneb mittedepolariseerivat tüüpi blokaad. See on seda tüüpi lihasrelaksantide nn teine toimefaas (varasem termin - "topeltblokk"). Teise toimefaasi mehhanism on siiani teadmata. On ilmne, et toime teist faasi saab seejärel elimineerida antikoliinesteraasi ravimitega ja tugevdada mittedepolariseerivate lihasrelaksantidega.
